《化妆品卫生规范》(2007年版)金黄色葡萄球菌检验
发布时间:2014-10-24 浏览次数:19343 分享:
1 范围 本规范规定了化妆品微生物学检验的基本要求。
本规范适用于化妆品样品的采集、保存及供检样品制备。
2 仪器和设备
2.1 天平。
2.2 高压灭菌器。
2.3 振荡器。
2.4 三角瓶,250mL。
2.5 玻璃珠。
2.6 玻璃棒。
2.7 刻度吸管,1mL、10mL。
2.8 研钵或均质器。
2.9 恒温水浴箱。
3 培养基和试剂
3.1 生理盐水
成分:
氯化钠 8.5g
蒸馏水加至1000mL
溶解后,分装到加玻璃珠的三角瓶内,每瓶 90mL,103.43kPa(121℃ 15 lb)20min
高压灭菌。
3.2 SCDLP 液体培养基
成分:
酪蛋白胨 17g
大豆蛋白胨 3g
氯化钠 5g
磷酸氢二钾 2.5g
葡萄糖 2.5g
卵磷脂 1g
吐温 80 7g
蒸馏水 1000mL
制法:先将卵磷脂在少量蒸馏水中加温溶解后,再与其它成分混合,加热溶解,调 pH
为 7.2~7.3 分装,103.43kPa(121℃ 15 lb)20min 高压灭菌。注意振荡,使沉淀于底层的 吐温 80 充分混合,冷却至 25℃左右使用。
注:如无酪蛋白胨和大豆蛋白胨,也可用多胨代替。
3.3 灭菌液体石蜡。
3.4 灭菌吐温 80。
3.5 7.5%的氯化钠肉汤
成分:
蛋白胨 10g
牛肉膏 3g
氯化钠 75g
蒸馏水加至 1000mL
制法:将上述成分加热溶解,调 pH 为 7.4,分装,103.43kPa(121℃ 15 lb)15min 高 压灭菌。
3.6 Baird Parker 平板
成分:
胰蛋白胨 10g
牛肉膏 5g
酵母浸膏 1g
丙酮酸钠 10g
甘氨酸 12g
氯化锂(LiCl·6H2O) 5g
琼脂 20g
蒸馏水 950mL
pH7.0±0.2
增菌剂的配制:30%卵黄盐水 50mL 与除菌过滤的 1%亚碲酸钾溶液 10mL 混合,保存 于冰箱内。
制法:将各成分加到蒸馏水中,加热煮沸完全溶解,冷至 25℃±1℃校正 pH。分装每瓶 95mL,103.43kPa(121℃ 15 lb)高压灭菌 15min。临用时加热溶化琼脂,每 95mL 加入 预热至 50℃左右的卵黄亚碲酸钾增菌剂 5mL,摇匀后倾注平板。培养基应是致密不透明的。 使用前在冰箱贮存不得超过 48h±2h。
3.7 血琼脂培养基
成分:
营养琼脂 100mL
脱纤维羊血(或兔血) 10mL
制法:将营养琼脂加热融化,待冷至 50℃左右无菌操作加入脱纤维羊血,摇匀,制成 平板,置冰箱内备用。
3.8 甘露醇发酵培养基
成分:
蛋白胨 10g
氯化钠 5g
甘露醇 10g
牛肉膏 5g
0.2%麝香草酚蓝溶液 12mL
蒸馏水 1000mL
制法:将蛋白胨、氯化钠、牛肉膏加到蒸馏水中,加热溶解,调 pH7.4,加入甘露醇和 指示剂,混匀后分装试管中,68.95kPa(115℃ 10 lb)20min 灭菌备用。
3.9 兔(人)血浆制备
取 3.8%柠檬酸钠溶液,103.43kPa(121℃ 15 lb)30min 高压灭菌,1 份加兔(人)全血 4 份,混匀静置;2000rpm~3000rpm 离心 3min~5min。血球下沉,取上面血浆。
4 样品的采集及注意事项
4.1 所采集的样品,应具有代表性,一般视每批化妆品数量大小,随机抽取相应数量的包装单位。检验时,应分别从两个包装单位以上的样品中共取 10g 或 10mL。包装量小于 20g
的样品,采样量可适当增加样品包装数量。
4.2 供检验样品,应严格保持原有的包装状态。容器不应有破裂,在检验前不得打开,防 止样品被污染。
4.3 接到样品后,应立即登记,编写检验序号,并按检验要求尽快检验。如不能及时检验, 样品应放在室温阴凉干燥处,不要冷藏或冷冻。
4.4 若只有一个样品而同时需做多种分析,如细菌、毒理、化学等,则宜先取出部分样品 做细菌检验,再将剩余样品做其它分析。
4.5 在检验过程中,从打开包装到全部检验操作结束,均须防止微生物的再污染和扩散, 所用器皿及材料均应事先灭菌,全部操作应在无菌室内进行,或在相应条件下,按无菌操作 规定进行。
4.6 如检出粪大肠菌群或其它致病菌,自报告发出之日起该菌种及被检样品应保存一个月。
5 供检样品的制备
5.1 液体样品
5.1.1水溶性的液体样品,可量取 10mL 加到 90mL 灭菌生理盐水中,如样品少于 10mL, 仍按 10 倍稀释法进行。如为 5mL 则加到 45mL 灭菌生理盐水,混匀后,制成 1:10 检液。
5.1.2油性液体样品,取样品 10mL,先加 5mL 灭菌液体石蜡混匀,再加 10mL灭菌的吐
温 80,在 40℃~44℃水浴中振荡混合 10min,加入灭菌的生理盐水 75mL(在 40℃~44℃ 水浴中预温),在 40℃~44℃水浴中乳化,制成 1:10 的悬液。
5.2 膏、霜、乳剂半固体状样品
5.2.1亲水性的样品:称取10g,加到装有玻璃珠及 90mL灭菌生理盐水的三角瓶中,充分 振荡混匀,静置 15min。用其上清液作为 1:10 的检液。
5.2.2疏水性样品:称取10g,放到灭菌的研钵中,加 10mL 灭菌液体石蜡,研磨成粘稠状, 再加入 10mL 灭菌吐温 80,研磨待溶解后,加 70mL 灭菌生理盐水,在40℃~44℃水浴中 充分混合,制成 1:10 检液。
5.3 固体样品
称取 10g,加到 90mL 灭菌生理盐水中,充分振荡混匀,使其分散混悬,静置后,取上 清液作为 1:10 的检液。
如有均质器,上述水溶性膏、霜、粉剂等,可称 10g 样品加入 90mL灭菌生理盐水, 均质 1min~2min;疏水性膏、霜及眉笔、口红等,称 10g 样品,加 10mL灭菌液体石蜡,
10mL 吐温 80,70mL 灭菌生理盐水,均质 3min~5min。
6 操作步骤
6.1 增菌:取 1:10 稀释的样品接种到 90mL SCDLP 液体培养基中,置36℃±1℃培养箱, 培养 24h±2h。
注:如无此培养基也可用 7.5%氯化钠肉汤。
6.2 分离:自上述增菌培养液中,取 1~2 接种环,划线接种在Baird Parker 氏培养基,如 无此培养基也可划线接种到血琼脂平板,置36℃±1℃培养 24h~48h。在血琼脂平板上菌落 呈金黄色,大而突起,圆形,不透明,表面光滑,周围有溶血圈。在 Baird Parker 氏培养基 上为圆形,光滑,凸起,湿润,直径为 2mm~3mm,颜色呈灰色到黑色,边缘为淡色,周 围为一混浊带,在其外层有一透明带。用接种针接触菌落似有奶油树胶的软度。偶然会遇到 非脂肪溶解的类似菌落,但无混浊带及透明带。挑取单个菌落分纯在血琼脂平板上,置 36℃±1℃培养 24h±2h。
6.3 染色镜检:挑取分纯菌落,涂片,进行革兰氏染色,镜检。金黄色葡萄球菌为革兰氏 阳性菌,排列成葡萄状,无芽胞,无夹膜,致病性葡萄球菌,菌体较小,直径约为 0.5m~1m。
6.4 甘露醇发酵试验:取上述分纯菌落接种到甘露醇发酵培养基中,在培养基液面上加入2mm~3mm的灭菌液体石蜡,置36℃±1℃培养 24h±2h,金黄色葡萄球菌应能发酵甘露醇 产酸。
5.5 血浆凝固酶试验:吸取 1:4 新鲜血浆 0.5mL,放入灭菌小试管中,加入待检菌 24h±2h 肉汤培养物 0.5mL。混匀,放36℃±1℃恒温箱或恒温水浴中,每半小时观察一次,6h 之内 如呈现凝块即为阳性。同时以已知血浆凝固酶阳性和阴性菌株肉汤培养物及肉汤培养基各0.5mL,分别加入灭菌 1:4 血浆 0.5mL,混匀,作为对照。
6 检验结果报告 凡在上述选择平板上有可疑菌落生长,经染色镜检,证明为革兰氏阳性葡萄球菌,并能
发酵甘露醇产酸,血浆凝固酶试验阳性者,可报告被检样品检出金黄色葡萄球菌。
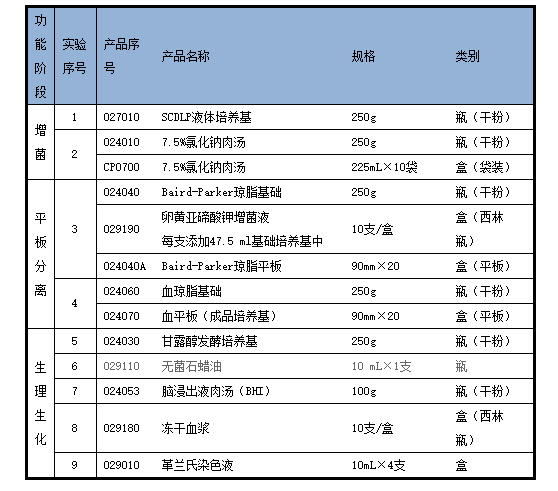
我公司针对标准的修改,扩充完善了微生物检测试剂,推出了成套的《化妆品卫生规范》(2007年版)金黄色葡萄球菌检验解决方案,为生产企业及检测机构(部门)提供方便。

图1:《化妆品卫生规范》(2007年版)金黄色葡萄球菌检验流程图