GB 4789.3-2025大肠菌群计数标准解读:实施要点、核心方法更新、操作细节、结果报告
发布时间:2025-12-03 浏览次数:1418
标准修订背景与实施要点
GB 4789.3-2025《食品安全国家标准 食品微生物学检验 大肠菌群计数》由国家市场监管总局发布,将于2025年9月16日正式实施,替代现行的GB 4789.3-2016标准。作为食品微生物检验的核心标准之一,此次修订历时多年,汇聚了行业专家与标准工作者的智慧结晶,不仅实现了与国际标准的进一步接轨,更在检测流程与结果报告方面实现了操作更灵活、方法更简便、效率更高效的全面提升。
大肠菌群作为食品卫生安全的关键指标菌,其检测结果直接影响企业对产品质量的把控和监管部门的执法决策。新标准通过吸纳国内外最新研究成果和实践经验,在结果处理、计数规则上做了更加科学、详细的规定,使检测结果更具准确性和可比性。此次修订标志着我国食品安全标准体系迈向更科学、更严谨、更完善的新阶段,为食品安全监管与行业高质量发展提供了坚实的技术支撑。
GB 4789.3-2025 主要修订内容概览
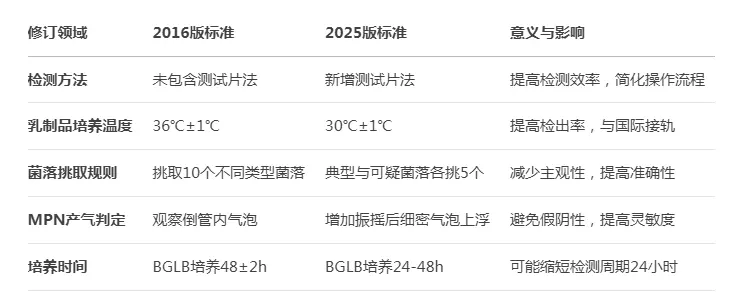
新标准的实施将给食品生产企业、检测机构和监管部门带来一系列操作变化和要求更新。企业和实验室需要在标准正式实施前完成方法验证、人员培训和设备调整等工作,以确保平稳过渡。
核心方法更新
1、测试片法的正式纳入
新标准最显著的创新之一是正式将大肠菌群计数测试片纳入标准方法体系,为食品微生物检测提供了更加便捷高效的技术选择。根据新标准规定,测试片的使用必须满足以下关键要求:
性能验证要求:测试片应以发酵乳糖产酸产气为阳性结果判断依据,且其性能必须符合GB 4789.28中相关培养基的质量要求。这一规定确保了测试片法的科学性和可靠性,避免了因方法差异导致的检测结果偏差。
操作便捷性优势:与传统VRBA培养基相比,测试片法无需繁琐的培养基配置步骤,操作更加简单直观。测试片凭借其即开即用的特性,大大缩短了实验准备时间,使整个检测流程变得更加高效。
结果判读标准化:新标准强调,无论使用传统方法还是测试片法,都必须以产酸产气作为阳性判断的根本依据,保持了不同方法间结果的一致性。
值得注意的是,在乳制品检测中,测试片法可能比传统平板法获得更高的计数结果。这是因为乳制品中可能存在不耐热或受损的大肠菌群,传统平板法在倾注过程中需要暴露于46℃左右的培养基中,导致部分敏感菌死亡;而测试片法没有这个受热过程,从样品处理到培养结束一直处于相对低的温度状态,因此检出率更高。
2、乳制品检测条件的专项优化
针对乳及乳制品的大肠菌群检测,新标准做出了一项重大调整:将平板计数的培养温度由原来的36℃±1℃修改为30℃±1℃。这一变更并非简单的参数调整,而是基于充分的科学研究和国际实践验证:
实验数据支持:标准修订过程中通过大量实验数据发现,无论是使用传统的VRBA平板计数还是测试片计数,乳及乳制品样品在30℃的培养条件下,计数结果均显著高于36℃的培养数值。这表明降低培养温度能够更有效地恢复和检测乳制品中可能存在的大肠菌群,提高结果的准确性和可靠性。
国际标准接轨:国际上权威的乳制品微生物检测标准普遍采用低于36℃的培养温度。例如,ISO 4832:2006标准规定使用30℃,FDA BAM Chapter 4(2020)标准采用32℃,而APHA(美国公共卫生协会)的乳品检验标准方法也推荐30℃~32℃的培养条件。这一调整实现了我国标准与国际主流标准的接轨,有利于实现"一次检测,全球通行"的目标。
行业影响深远:这一变更直接关联《食品安全国家标准 干酪》(GB 5420-2021)、《食品安全国家标准 发酵乳》(GB 19302-2010)等多项乳制品产品标准的实施。乳制品企业需要特别关注这一变化,及时调整实验室培养条件,确保检测结果符合新标准要求。
3、MPN法的优化与完善
新标准对MPN(最可能数)法进行了多项技术性优化,提高了方法的可操作性和结果准确性:
产气现象的明确定义:新标准将MPN法中产气现象的判定标准修改为:"小导管或产气收集装置内有气泡产生,或轻轻摇振试管可见有细密气泡不断上升者判断为产气"。这一修订解决了实际操作中的一个常见难题——有时细菌产气量少,气体会溶解于液体中,导致倒管内无法观察到明显气泡。通过增加振摇试管观察细密气泡上浮的判定方法,显著降低了假阴性结果的风险。
培养时间灵活调整:复发酵试验中BGLB肉汤培养基的培养时间由原来的固定"48±2h"修改为"24-48h",并规定"若24h可得到阳性结果,则可停止培养"。这一变化使检验周期最多可缩短24小时,提高了检测效率,尤其有利于食品企业加快产品放行速度。
操作时间严格管控:新标准明确规定,从制备样品匀液开始至接种到LST肉汤管完毕的全过程不得超过15分钟。这一严格的时间控制要求旨在避免样品在处理过程中因时间延长而导致微生物状态改变,确保检测结果真实反映样品初始状况。
双料肉汤使用规范:标准进一步明确了双料LST肉汤的使用规则:"如接种体积超过1mL,则加到等体积的双料LST肉汤中"。这一规定消除了实际操作中的模糊地带,为不同接种量提供了明确的操作指引。
操作细节优化
1、菌落挑取规则的细化
新标准针对平板计数法中菌落挑取这一关键操作环节,作出了更加明确和细化的规定,解决了以往检测人员在实际操作中的困惑:
分类挑取原则:按照GB 4789.3-2016的要求,检测人员需要"挑取10个不同类型的典型和可疑菌落",但对于"不同类型"的具体含义存在理解差异——是指长得不一样的可疑菌落,还是典型和可疑的菌落随意选择?新标准彻底解决了这一歧义,明确规定:"典型和可疑菌落分开计数,各挑取5个验证"。这一变化使操作规范更加清晰,减少了不同实验室间的操作差异。
科学依据:这一修订是基于大量实验观察和数据统计。研究表明,在VRBA平板上出现的非典型菌落(偏小或晕环不明显)经过鉴定,95%以上都不是大肠菌群;而典型菌落(红色至紫红色,带明显胆盐沉淀环)是大肠菌群的概率则高得多。分开计数和验证能够更准确地反映样品中大肠菌群的实际数量。
补充规定:当平板上典型或可疑菌落数量不足5个时,新标准要求挑取全部菌落进行验证。这确保了即使菌落数较少时,也能获得可靠的确认结果。
2、培养基处理与培养条件调整
新标准在培养基制备和培养条件方面进行了多项技术参数优化,提高了实验的稳定性和可重复性:
VRBA保温温度调整:新标准将VRBA培养基的水浴保温温度由原来的"46±2℃"提高到"48±2℃"。这一调整考虑了不同实验室环境条件差异和不同品牌琼脂产品的凝固点变化,提高水浴温度可有效减少琼脂在倾注前凝固的现象,保证培养基流动性。但同时标准也提醒,实际操作时倾注培养基的温度不宜过高,否则可能导致热敏感菌受损,造成计数结果偏低。
乳制品培养专项规定:针对乳及乳制品的培养条件,新标准在多个环节进行了补充和强化。除温度调整外,还明确规定:"对于乳及乳制品,应置于30℃±1℃培养18h~24h",并在检验程序图中也相应增加了这一特殊要求。
培养观察细节完善:新标准对培养后的菌落观察提出了更细致的要求,必要时需使用放大镜或菌落计数器,并特别说明在菌落数选择时应"选取所有菌落数在15CFU~150CFU之间的平板",与旧版标准的表述有所区别。
表:关键操作要求变化对比
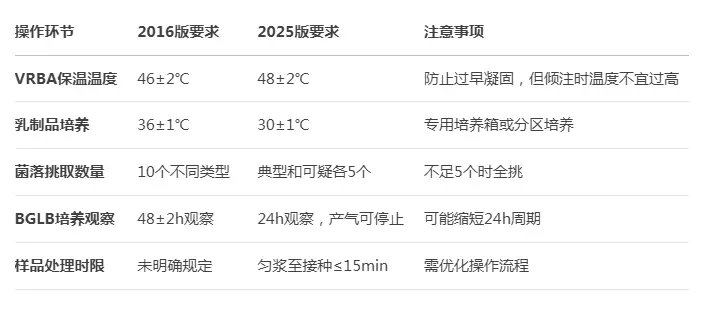
3、时间控制与操作流程强化
新标准在多处强化了时间控制要求,确保检测过程不会因操作延迟影响结果准确性:
严格时限规定:除了前述MPN法中"从制备样品匀液至接种到LST肉汤管完毕全过程不得超过15min"的要求外,在平板计数法中也同样规定"从制备样品匀液开始至倾注VRBA完毕,全过程不得超过15min"。这一严格的时间约束要求实验室必须优化操作流程,提前准备好所有试剂和设备,确保样品处理高效进行。
流程衔接优化:新标准在样品处理环节增加了灵活性,特别是对于液体样品,规定"当样品不适宜进行体积取样时,按固体和半固体样品称重操作"。这一补充解决了某些粘稠或含颗粒液体样品难以准确量取体积的问题,扩大了标准适用范围。
稀释操作调整:新标准取消了稀释过程中"换用吸管吹打"的硬性规定,给予实验室更多操作灵活性。同时,在附录部分增加了"附录C 确定最适的3个连续稀释度方法",解决了当检测样品含菌量不确定时,如何选择计算稀释度的问题。
结果计算与报告规范
1、新增附录与示例说明
新标准通过增加附录内容的方式,大大完善了结果计算与报告部分的规范性和可操作性:
附录D的补充:新增的"附录D 大肠菌群平板计数结果处理及示例"详细规定了菌落数的计算、数值修约和结果报告的具体方式,并提供了多种情形的示例说明。这一补充特别有助于解决实际检测中的复杂情况,如:
① 双稀释度平板菌落数均在15-150CFU之间时的处理方式
② 所有平板菌落数均低于15CFU或高于150CFU时的计算方法
③ 空白对照出现菌落生长时的处理方案
计算规则细化:新标准明确要求,当同一稀释度的两个平板中,一个平板有典型菌落生长而另一个没有时,应以有菌落生长的平板计算该稀释度的菌落数。这种细节规定避免了因单板无菌落而误判的情况,更加科学合理。
数字修约规范:新标准在结果报告部分明确规定了"四舍五入"的修约原则,统一了结果报告方式,提高了不同实验室间结果的可比性。
2、MPN检索表的扩展与优化
新标准对MPN检索表进行了功能性扩展,使其更加实用和全面:
单位换算补充:在MPN检索表中增加了MPN/g(mL)与MPN/100g(mL)的换算说明,明确指出"把表中的数值乘以100就可以"实现单位转换。这一补充解决了某些特定产品标准(如历史标准或出口要求)中可能使用不同单位的问题,提高了标准的兼容性。
阳性管组合处理:新标准在结果与报告部分规定,当连续的稀释度超过3个时,应"根据附录C确定最适的3个连续稀释度"。新增的附录C提供了具体的筛选原则和方法,解决了实际检测中因样品含菌量不确定而需设置多个稀释度时的结果计算问题。
贝类产品专项要求:虽然主要在大肠埃希氏菌计数标准(GB 4789.38-2025)中体现,但新标准体系对特殊产品如贝类设置了专门的检测要求和检索表。这体现了标准修订中对不同产品特性的充分考虑。
实施建议
1、检验检测机构应用策略
面对新标准的变化,检测机构需要采取系统性策略确保顺利过渡:
方法验证与确认:根据《检验检测机构资质认定评审准则》和CNAS-CL01《检测和校准实验室能力认可准则》要求,实验室应对变更后的标准方法重新进行验证。验证内容应包括但不限于:
① 测试片法与传统方法的比对
② 30℃与36℃培养条件下乳制品检测结果的差异分析
③ 新判定规则下的阳性率变化
设备与材料准备:检验检测机构需评估现有设备是否满足新要求,特别是:
① 30℃恒温培养箱(用于乳制品检测)
② 符合标准要求的大肠菌群计数测试片
③ 温度范围调整的恒温水浴箱(48±2℃)
人员培训重点:针对标准主要变化点开展专项培训,重点包括:
① 测试片法的标准化操作
② 乳制品30℃培养的专项流程
③ 新版菌落挑取规则与结果计算
④ MPN法产气判定的新标准(振摇观察)
文件体系更新:及时修订:
① 实验室作业指导书
② 记录表格(体现典型/可疑菌落分开记录等新要求)
③ 报告格式(增加测试片法说明等)
2、实验室验证要点
为确保新标准检测结果的准确性和可靠性,实验室应重点关注以下验证环节:
测试片方法验证:
① 与参考方法(VRBA平板法)进行平行比对,使用不同类型食品样品
② 验证测试片保存条件和有效期对结果的影响
③ 确认测试片的选择性和分辨率是否符合要求
温度调整验证:
① 针对乳制品,设计30℃与36℃培养的对比试验
②使用标准菌株(如大肠埃希氏菌ATCC 25922)验证不同温度下的回收率
③ 分析温度变化对不同种类大肠菌群检出率的影响
临界样本分析:
① 制备接近限值标准的样品(如合格/不合格临界点)
② 验证新标准下结果判定的准确性和重复性
③ 分析菌落挑取规则变化对低污染度样品结果的影响
质控样品应用:
① 使用CICC等机构提供的标准菌株(如大肠埃希氏菌、克雷伯氏菌等)和定量质控样品
② 建立阳性对照和阴性对照体系
③ 进行实验室间比对或参加能力验证计划
GB 4789.3-2025的发布实施是我国食品安全标准体系不断完善的重要体现。通过吸纳科学研究成果和国际先进经验,新标准在检测效率、结果准确性和国际兼容性方面取得了显著进步。检验检测机构应当充分重视标准变化,提前做好技术准备和人员培训,确保在2025年9月16日标准正式实施后能够及时符合新要求,为食品安全保障提供更加科学可靠的技术支撑。
本文由环凯转载自“芝罘疾控”公众号,版权归原作者所有,仅供学习参考,如有侵权请联系删除!











