解读中国药典 9205 药品洁净实验室微生物监测和控制指导原则
发布时间:2026-01-20 浏览次数:1184
引言:洁净实验室的 “微生物防线”,为何成为药企合规关键?
药品质量的底线,藏在每一个洁净实验室的微生物控制细节里。作为药品无菌检验与微生物检测的核心场所,洁净实验室的环境稳定性直接决定检测结果准确性与药品安全性。2025 版《中国药典》正式实施后,通则 9205《药品洁净实验室微生物监测和控制指导原则》迎来关键修订,新增动态风险管理要求、补充物理参数监测维度、优化监测流程规范,为药企建立科学合规的微生物控制体系提供了明确指引。
本文将从核心修订、条款解读、实操要点三大维度,带您全面掌握 9205 指导原则的合规逻辑与落地方法。
一、2025 版 9205 指导原则核心修订亮点
相较于 2020 版,新版指导原则更强调 “主动控制” 与 “风险量化”,核心变化集中在 4 大方向:
1. 物理参数监测维度扩容
新增照度、噪音两项确认与监测要求,与原有高效过滤器完整性、气流组织、风速、换气次数、压差、温湿度等参数共同构成 “全维度物理指标体系”。其中,A 级洁净区高效过滤器完整性监测周期为 24 个月,温湿度需每次实验监测(控制在 20-24℃、45-65% RH),压差要求洁净区与非洁净区、不同级别洁净区之间均不小于 10Pa。
2. 监测计划的系统化升级
明确要求实验室必须建立 “全要素监测计划”,包含取样位置、监测状态(静态 / 动态)、频次、方法、培养条件等核心内容,首次强制要求制定警戒限与纠偏限,并建立数据趋势分析及偏差处理机制,将被动监测升级为主动风险预警。
3. 术语与流程的精准优化
将 “重新验证” 调整为 “重新确认”,明确当超净工作台、空调系统等关键设备发生重大变更,或监测结果出现偏离时,需重新进行参数测试与微生物监测,强化流程的可操作性与合规性。
4. 培养条件的灵活化调整
微生物监测用培养箱及培养条件不再强制统一,允许实验室根据检测需求灵活设定,但需通过验证确保方法的科学性与可靠性,兼顾合规性与实际应用场景适配性。
二、9205 指导原则核心条款深度解读
(一)洁净实验室分级与适用场景
指导原则明确,药品洁净实验室按空气悬浮粒子标准分为 A、B、C、D 四个级别,各级别静态 / 动态悬浮粒子与微生物控制标准如下:
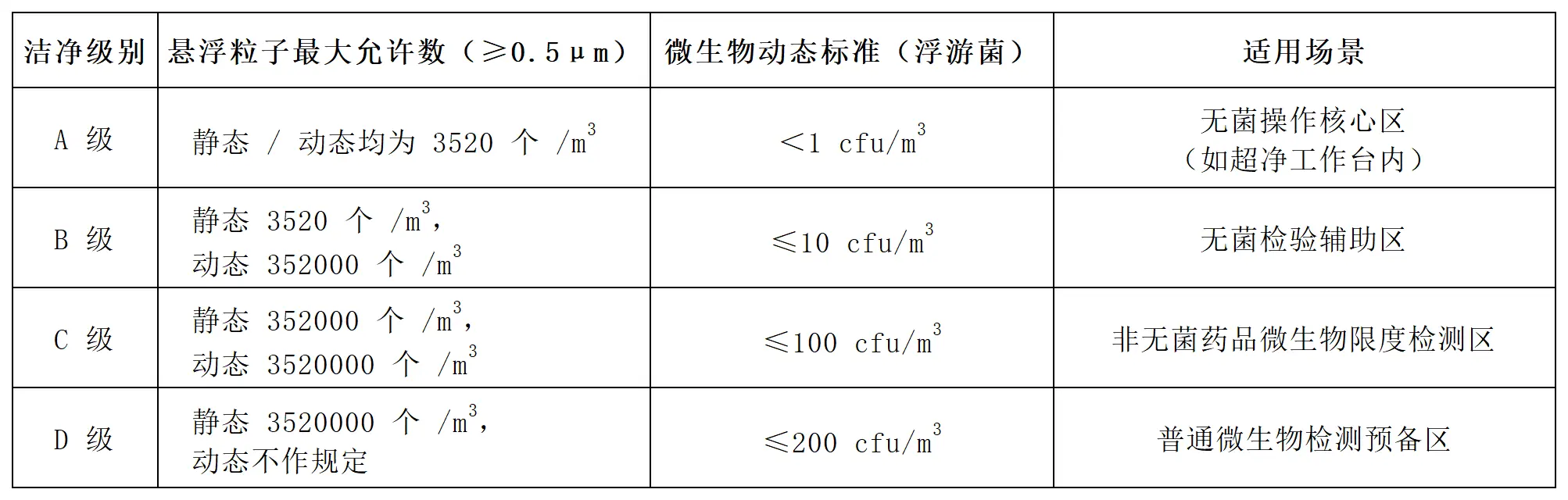
注:表面微生物控制标准中,A 级接触碟法≤1 cfu / 碟,5 指手套≤1 cfu / 手套;B 级分别为≤5 cfu / 碟、≤5 cfu / 手套。
(二)监测方法与频次要求
1. 三大核心监测项目与方法
空气悬浮粒子:参照《医药工业洁净室 (区) 悬浮粒子的测试方法》,取样点需具有代表性,单次取样量不低于 2 升,取样时间不少于 1 分钟,A 级每次实验监测,B 级每季度监测,C/D 级每半年监测。
微生物监测:包含浮游菌(撞击式 / 滤膜式采样)、沉降菌(φ90mm 培养皿暴露 4 小时),培养基优先选用 TSA(胰酪大豆胨琼脂),疑似真菌污染时可加用 SDA(沙氏葡萄糖琼脂)。
表面微生物:规则表面用接触碟法(25cm²/ 碟),不规则表面(如设备缝隙)用擦拭法(25cm²/ 拭子),实验结束后取样检测,重点监测台面、操作服、手套等关键接触面。
2. 推荐监测频次(核心场景)
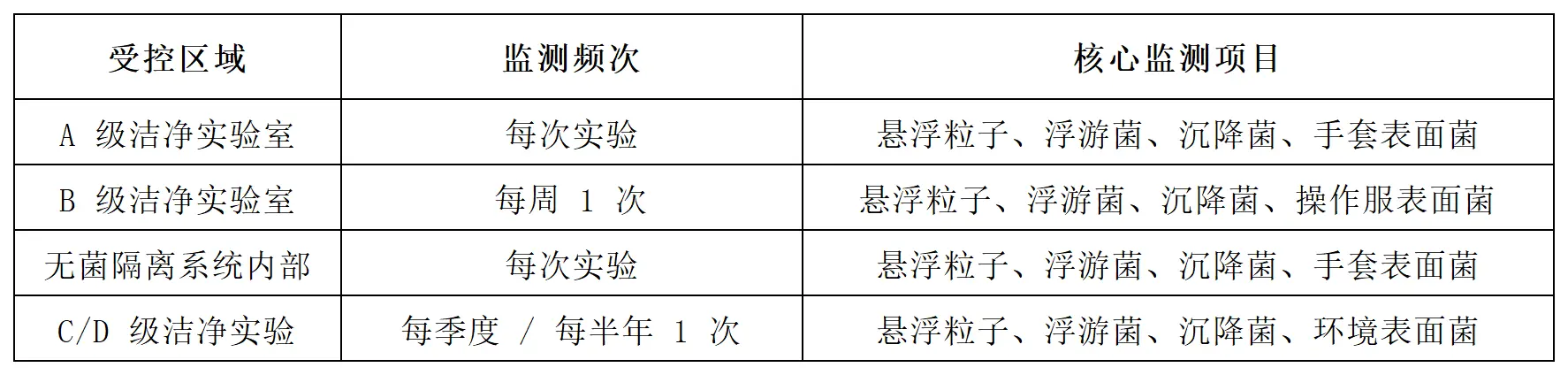
注:当出现连续超警戒限、设备重大维修、区域结构变更等情况,需加密监测频次。
(三)人员与确认要求
人员资质:需符合《中国药典》通则 9203《药品微生物实验室质量管理指导原则》,具备微生物监测专业能力,熟悉监测流程与偏差处理要求。
初次确认:新建成或初次使用的洁净实验室,需完成物理参数、悬浮粒子、微生物三项核心确认,测试先静态后动态,确保系统运行可靠后再开展正式检测。
三、合规落地实操要点:从标准到执行
1. 建立 “分级分类” 监测体系
根据洁净级别差异制定差异化方案:A 级区聚焦实时监控(如在线粒子计数器),B 级区强化每周巡检,C/D 级区按季度 / 半年开展全面检测,同时结合药品特性(如无菌制剂、生物制品)增加关键点位监测频次。
2. 科学设定警戒限与纠偏限
基于历史监测数据(建议至少 12 个月),用统计方法(如均值 ±2 标准差)制定阈值:警戒限为 “需关注的预警线”,触发后启动趋势分析;纠偏限为 “必须干预的行动线”,触发后立即暂停检测,排查污染源(如过滤器泄漏、人员操作不当),清洁消毒后重新监测合格方可恢复使用。
3. 强化设备与环境维护
高效过滤器:定期扫描检漏,发现泄漏立即更换,更换后重新确认气流组织与洁净度;
清洁消毒:采用 “消毒 - 清洁 - 消毒” 双循环流程,选用符合 GMP 要求的消毒剂,避免微生物耐药性;
人员管理:进入洁净区需按规范更衣(无菌服、手套、口罩全覆盖),定期开展人员微生物污染监测(如手套擦拭取样)。
4. 做好数据分析与偏差记录
建立电子台账记录所有监测数据,定期开展趋势分析(如月度 / 季度数据对比),识别潜在风险;偏差处理需遵循 “发现 - 评估 - 调查 - 纠正 - 预防” 闭环,记录污染原因、处理措施、验证结果,确保可追溯。
结语:以标准为纲,筑牢药品质量防线
2025 版 9205 指导原则的实施,标志着我国药品洁净实验室微生物控制从 “合规达标” 向 “风险可控” 的进阶。对于药企而言,不仅需要吃透标准条款,更要将其转化为可落地的日常操作流程 —— 通过建立全维度监测体系、科学设定风险阈值、强化人员与设备管理,让洁净实验室真正成为药品质量的 “安全屏障”。
合规之路无捷径,细节之处见真章。遵循 9205 指导原则的核心逻辑,将微生物控制融入每一个实验环节,既是满足药典要求的必然选择,更是守护公众用药安全的责任担当。
本文由环凯转载自“检验视界君”公众号,版权归原作者所有,仅供学习参考,如有侵权请联系删除!