产品名称:诺如病毒GI/GII核酸检测试剂盒(RT-PCR探针法,含MS2)
英文名称:Norovirus (GI/GII) Real Time RT-PCR Kit (with MS2)
产品编号与包装规格:
| 编号 | 规格 |
|---|---|
| FZ028BF2 | 48 测试/盒 |
产品简介:本试剂盒适用于贝类,硬质食品表面,软质水果以及水中诺如病毒的定性检测,不可用于临床诊断。
检测原理:本试剂盒采用一步法实时荧光RT-PCR技术,针对诺如病毒GI/GII型特异性基因序列设计高灵敏度引物及探针。在PCR扩增过程中,探针与靶标基因结合后被Taq酶水解,释放荧光信号。荧光定量PCR仪实时监测FAM(GI型)、VIC(GII型)及ROX(MS2噬菌体内标)三个荧光通道的扩增曲线,通过对数期荧光信号的动态变化实现诺如病毒核酸的定性检测,并同步监控实验有效性。
诺如病毒GI/GII核酸检测试剂盒(RT-PCR探针法,含MS2)产品组分:
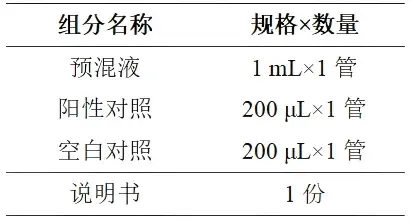
注1:预混合液含有引物和探针等反应成分,不含ROX;本试剂盒不含病毒富集试剂及RNA提取试剂。
注2:空白对照为RNase-free ddH2O;阳性对照为含有检测基因的DNA片段;阴性对照为阴性样本提取的RNA,不提供。
储存条件与保质期:-20℃避光储存,避免反复冻融。有效期为12个月,生产日期见外包装。
灵敏度:最低检验限达到10-100 copies/Test
所需其他材料和适用仪器:本试剂盒适用于ABI系列、Bio-Rad系列等实时荧光定量PCR仪(具有能够检测FAM、VIC和ROX标记的荧光通道)。
诺如病毒GI/GII核酸检测试剂盒(RT-PCR探针法,含MS2)检测方法:
1,病毒富集:贝类,硬质表面食品,软质水果等样品可参照《GB4789.42-2025 食品安全国家标准 食品微生物学检验 诺如病毒检验》,水样品可参照《ISO 15216-2 2019 Microbiology of the food chain Horizontal method for determination of hepatitis A virus and norovirus using real-time RT-PCR》。
2, 样本制备及RNA提取:样品按照病毒RNA提取试剂盒相应要求和步骤提取,也可手工提取和纯化或使用自动化的提取仪器。
3, 反应体系配置
从试剂盒中取出预混合液和酶混合液,充分融化,轻微振荡混匀,瞬时离心。
按照下表等比例配置反应体系,预混液20 μL置于PCR管或PCR板中,然后将空白对照、样品RNA提取液、阳性对照各取5 μL分别加入PCR管或PCR板中,盖好管盖或板膜,短暂离心后立即进行PCR扩增反应。
4, PCR扩增:PCR管或PCR板置于PCR仪器上,推荐反应程序设定如下:反应体系25 μL,在第三步每个循环60℃时检测荧光信号,检测通道选择FAM、VIC和ROX。

注:使用ABI系列PCR仪器,如果不添加ROX,“passive reference”和“quencher”均选择“none”。
5、标准曲线绘制:绝大多数PCR仪都能够自动生成标准曲线,如未生成,可以未稀释和梯度稀释的MS2过程控制的浓度lg值为X轴(设过程控制病毒原液浓度为1),以其Ct值(部分PCR仪显示为Cq)为Y轴,绘制过程控制标准曲线。
6、质量控制
满足以下条件本次检测有效:
1)空白对照和阴性对照无扩增曲线;
2)MS2过程控制在相应的检测通道有S型扩增曲线且标准曲线R2≥0.98;
3)阳性对照(GI过程控制和GII过程控制)在相应的检测通道有S型扩增曲线;
4)提取效率≥1%;
5)抑制指数<2.0。
注1:如果对照满足质量控制要求,提取效率与抑制指数不满足质量控制要求,检测结果为阳性时也可酌情判定为阳性。
注2:如果除空白和阴性对照外,其他对照满足质量控制要求,提取效率与抑制指数也满足质量控制要求,检测结果为阴性时也可酌情判定为阴性。
注3:设样本经过前处理后获得的病毒富集液总体积为V1,从V1中取出进行RNA提取的体积为V2,最终溶解或洗脱RNA时使用的液体体积为V3。将MS2初始浓度设为1,假设样本原液外加扩增控制的抑制指数小于2,实际样本检测时MS2的Ct值在标准曲线上对应的浓度为C(如果仪器未生成标准曲线,需将Ct值带入绘制的标准曲线计算对应浓度的lg值),则提取效率=(C×V1×V3)/(10×V2×1)×100%。
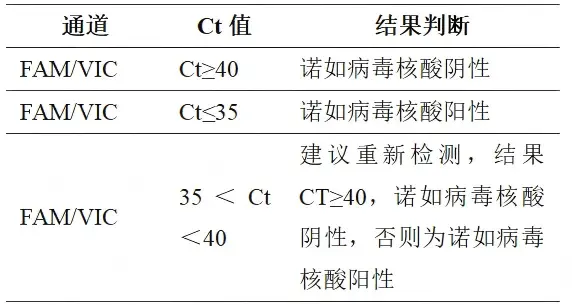
7、结果分析及判定:在检测有效的情况下,如下表进行判定,其中FAM通道为诺如病毒GI检测结果,VIC通道为诺如病毒GII检测结果,ROX通道为MS2过程控制检测结果。