微生物分离纯化的6种分离方法和各国药典的技术要求
发布时间:2026-01-22 浏览次数:718
微生物分离纯化是指从混杂微生物群体中获得仅含单一物种或菌株纯培养物的过程,此过程是微生物鉴定、药品微生物质量控制、临床病原学诊断及微生物学基础研究的核心基石。2025版《中华人民共和国药典》(以下简称ChP 2025)对微生物分离纯化的技术规范性、方法适用性验证及质量控制提出了更为严谨的要求,与美国药典(USP)、欧洲药典(EP)、英国药典(BP)、日本药典(JP)共同构建了全球化的微生物检验标准体系。本文系统阐述倾注平板法、涂布平板法、平板划线法、富集培养法、厌氧法及单细胞分离法6种经典技术的操作流程、适用范围、优缺点及注意事项,对比各国药典在培养基选择、培养条件、方法验证等方面的异同,分析GMP视角下的重点难点与风险控制要点,旨在为微生物专业人员提供兼具理论深度与实操指导性的专业参考。
一、微生物分离纯化的技术内涵
含有一种以上微生物的培养物称为混合培养物,若一个菌落中所有细胞均源自一个亲代细胞,则该菌落称为纯培养物。在进行菌种鉴定、药敏试验、代谢产物研究等工作时,所用微生物必须为纯培养物,而获得纯培养物的过程即为分离纯化。该过程的本质是通过物理或化学手段使微生物个体在空间上充分离散,同时提供适宜的营养、温度、pH及气体环境,或利用选择性培养基抑制非目标微生物生长,促使目标微生物独立增殖形成单菌落,进而通过挑取单菌落实现纯化。
贯穿分离纯化全过程的核心是无菌操作技术,其涵盖操作环境的洁净控制、器具的灭菌处理、操作过程的污染防控等关键环节。所有操作需在经紫外灭菌的超净工作台或无菌操作室内进行,常用灭菌方式包括高压蒸汽灭菌、火焰灼烧灭菌、酒精擦拭消毒等,任何无菌操作的疏漏都将直接导致分离纯化失败,这是ChP 2025及各国药典均着重强调的技术前提。
二、六种经典微生物分离纯化技术的实操
一)倾注平板法
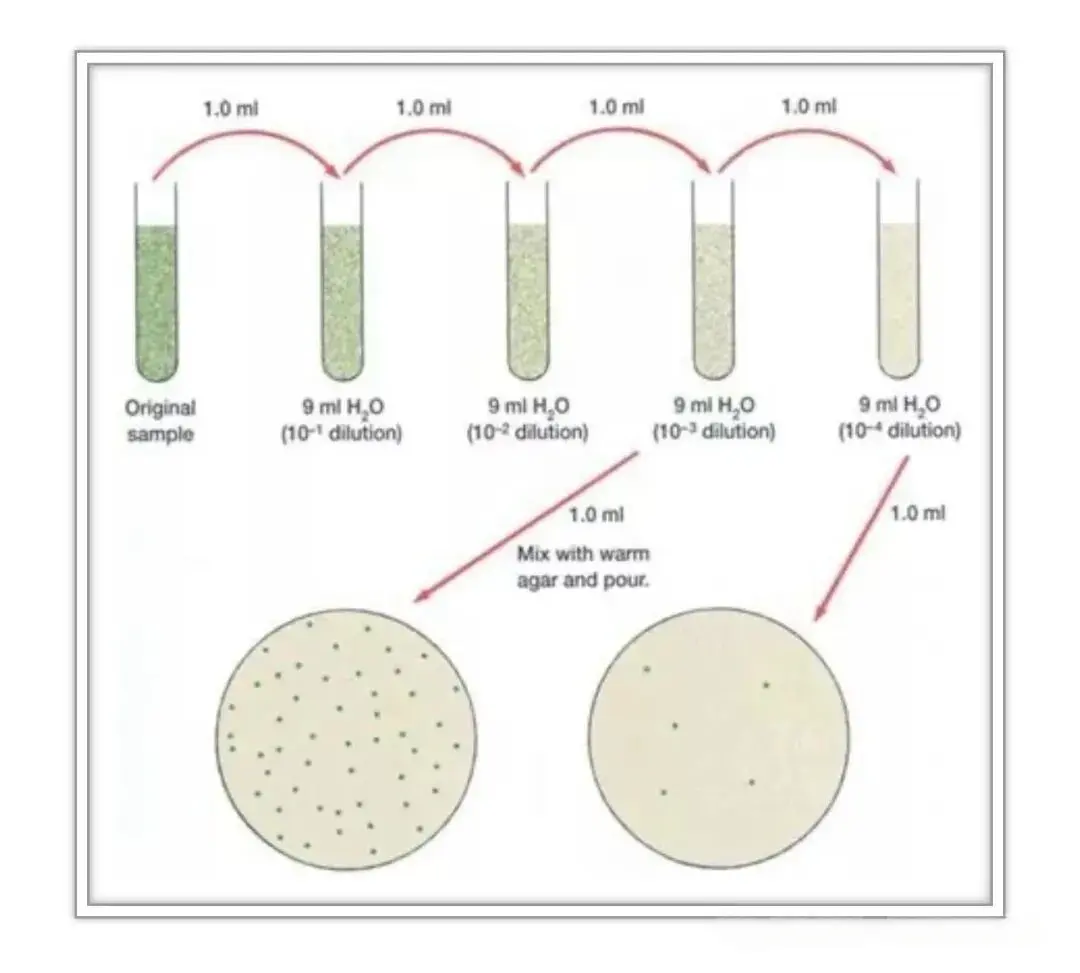
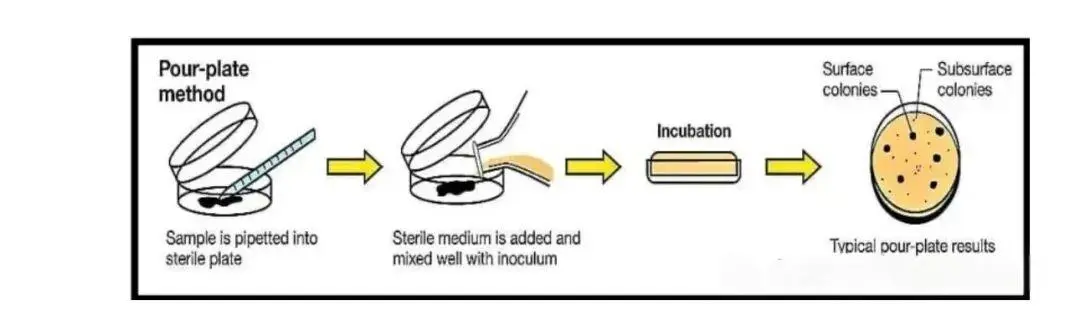
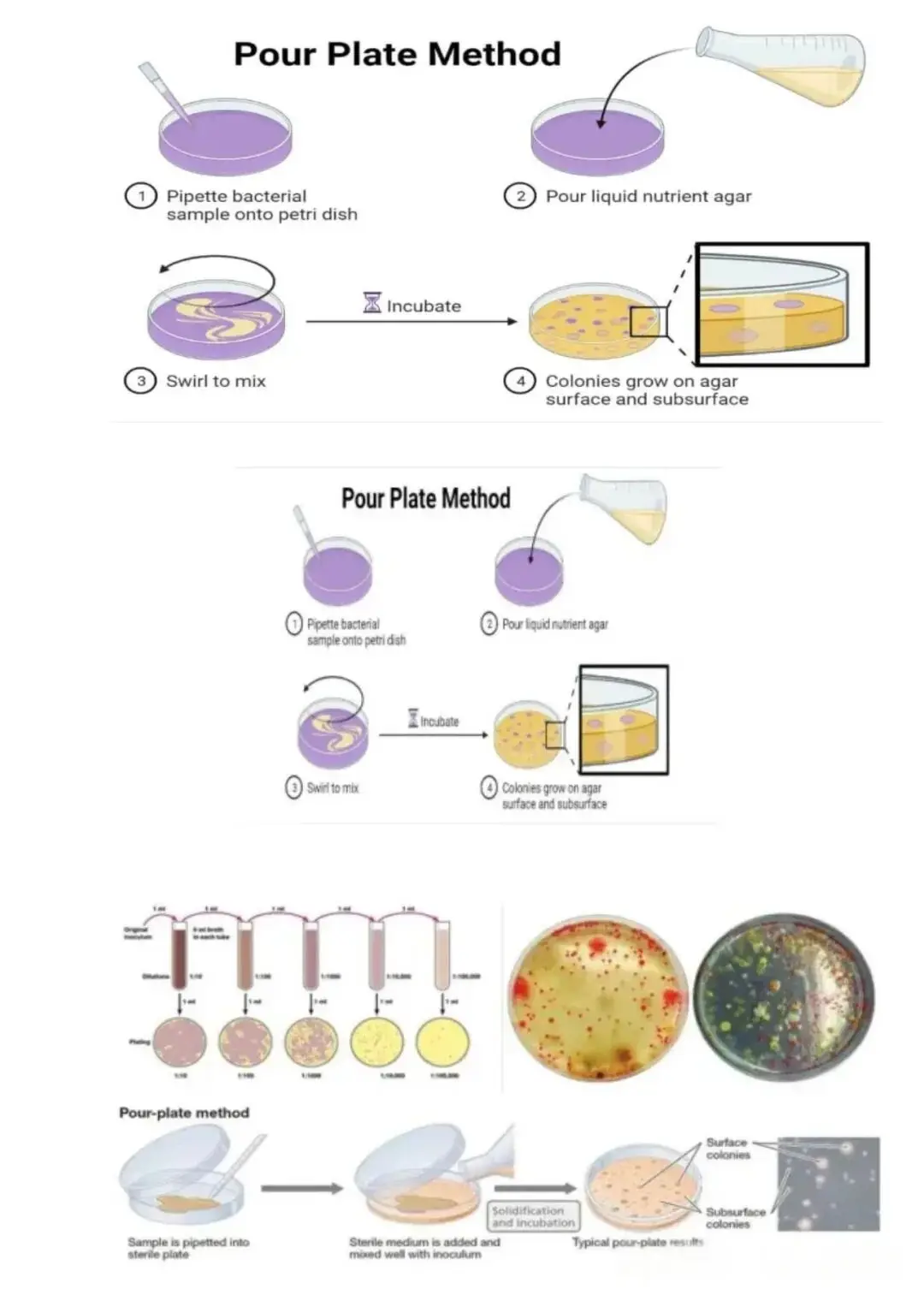
倾注平板法的核心操作流程为,将待测微生物悬液进行系列梯度稀释后,吸取定量稀释液注入无菌培养皿,随即倾入已熔化并冷却至40-50℃的无菌营养琼脂培养基,轻轻旋转培养皿使菌液与培养基充分混匀,待琼脂完全凝固后倒置放入恒温培养箱培养。培养后,微生物菌落既生长于培养基表面,也分布于培养基内部,挑取单个菌落制成悬液并重复上述操作数次,即可获得纯培养物。
该方法的适用范围以需氧及兼性厌氧微生物的活菌计数为主,同时可用于分离能在琼脂内部生长的微生物,尤其适用于样品中菌落形成单位(CFU)数量较高的场景。其优点在于操作简便,菌液与培养基混合均匀,菌落分布相对均一,定量结果准确性较高;缺点则是需严格控制琼脂温度,温度过高易导致微生物死亡,温度过低则培养基提前凝固造成混合不均,且挑取深层菌落的操作难度大于表面菌落,同时对严格好氧菌的分离效果欠佳。
操作注意事项需重点关注三点,一是融化后的琼脂培养基需冷却至手握不烫手的温度,避免高温损伤微生物;二是倾注与混匀过程需轻柔迅速,防止培养基溅出或产生气泡影响菌落观察;三是培养阶段必须倒置平板,防止冷凝水滴落冲散菌落。
二)涂布平板法
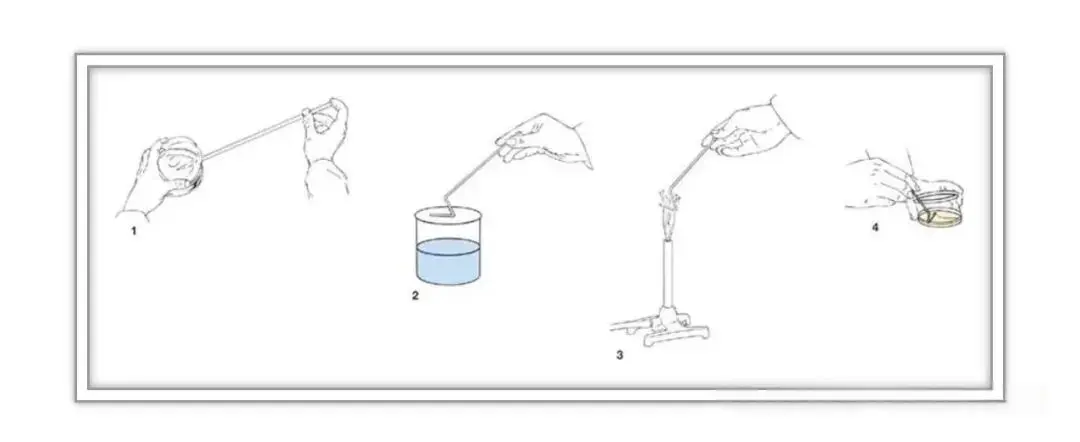
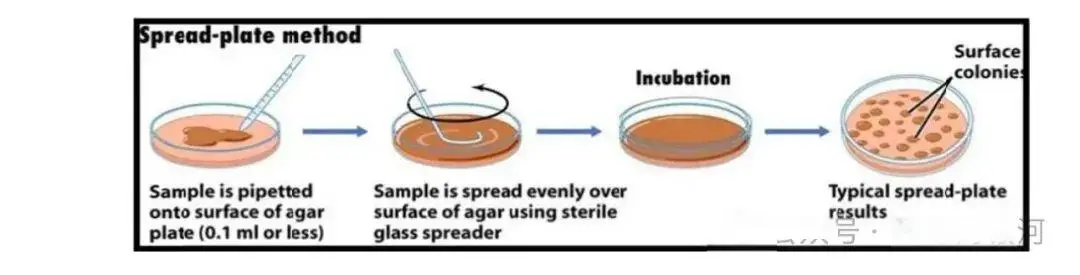
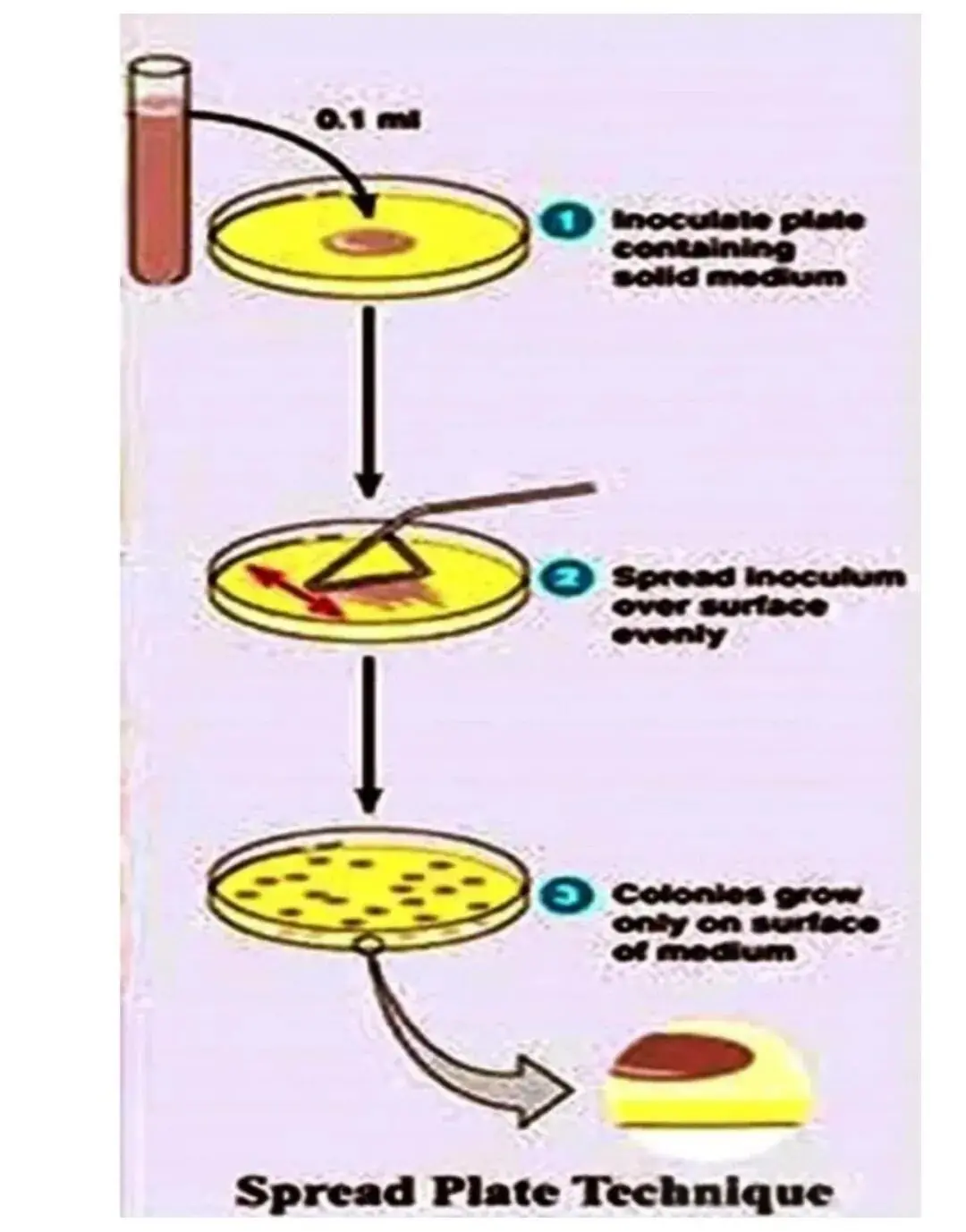
涂布平板法的操作流程为,将微生物悬液进行适当梯度稀释后,吸取0.1mL左右的稀释液垂直滴加至已凝固的无菌固体琼脂平板中央,使用无菌玻璃涂布棒将菌液均匀涂布于培养基表面,涂布时可缓慢旋转培养皿以确保菌液覆盖整个平板,静置数分钟待菌液被培养基完全吸收后,倒置进行恒温培养。
该方法适用于好氧及兼性厌氧微生物的分离纯化、活菌计数及菌落形态观察,特别适合需要对菌落进行后续操作如药敏试验、形态学鉴定的实验场景。其优点是所有菌落均生长于培养基表面,形态特征清晰易辨,便于挑取和观察,且涂布过程对微生物的热损伤较小;缺点是对操作人员的涂布技术要求较高,涂布不均易造成菌落堆积或分布稀疏,同时不适用于严格厌氧菌的分离,对粘稠样品的分散效果较差。
操作注意事项包括,一是涂布棒使用前后需经酒精浸泡并火焰灼烧灭菌,且必须冷却至室温后再接触菌液,避免高温杀死微生物;二是菌液滴加量不宜过多,过量菌液难以被培养基吸收,易导致涂布不均;三是涂布时力度需轻柔,防止划破培养基表面影响菌落生长。

三)平板划线法
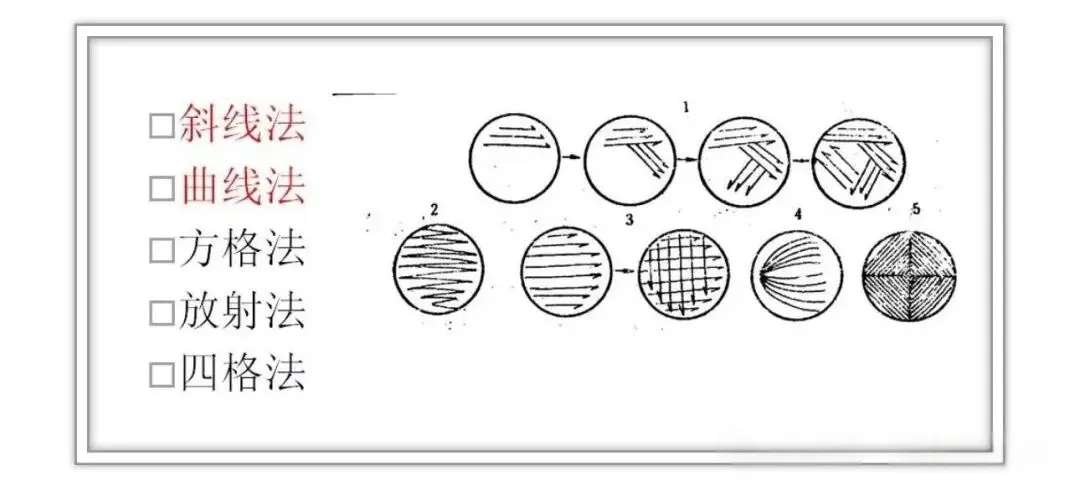
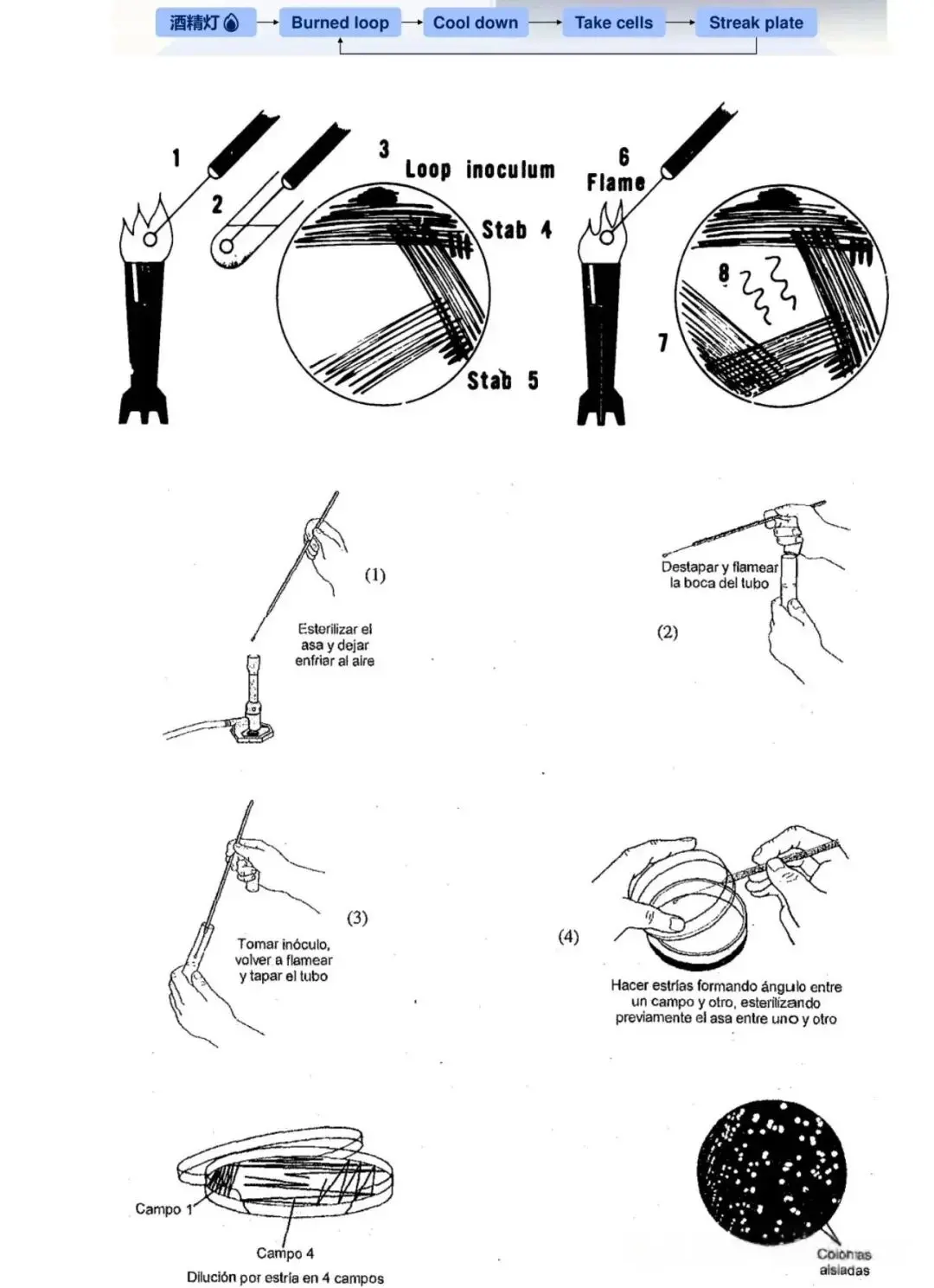
平板划线法是最简单且常用的微生物分离方法,操作流程为,将接种环经火焰灼烧灭菌并冷却后,蘸取少量待分离的微生物培养物,在无菌固体琼脂平板表面进行规律性划线,常见划线方式包括斜线法、曲线法、方格法、放射法及四格法等。随着划线次数增加,接种环上的菌液浓度逐渐降低,最终在划线的末端区域实现微生物细胞的充分离散,经恒温培养后形成单个菌落。
该方法适用于绝大多数可培养微生物的初步分离纯化,尤其适合从混合培养物中快速分离单菌落,是微生物实验室日常纯化工作的基础方法。其优点在于操作快速简便,无需复杂的梯度稀释步骤,实验成本低廉;缺点是分离效果高度依赖操作人员的技术熟练度,划线手法不当易造成菌落交叉污染或无法形成单菌落,对于微生物浓度极高的样品,需预先进行稀释处理。
操作注意事项需严格遵循无菌操作原则,一是每次划线前后均需对接种环进行灼烧灭菌,且灭菌后需在培养基边缘冷却,避免高温烫死微生物;二是划线时接种环与平板表面保持适宜角度,力度轻柔,仅以接种环尖端接触培养基表面滑动,切勿刺入琼脂内部;三是采用分区划线法时,每一区划线结束后必须灼烧接种环,且下一区的划线需从上一区的末端开始,以达到有效稀释菌液的目的。

四)富集培养法
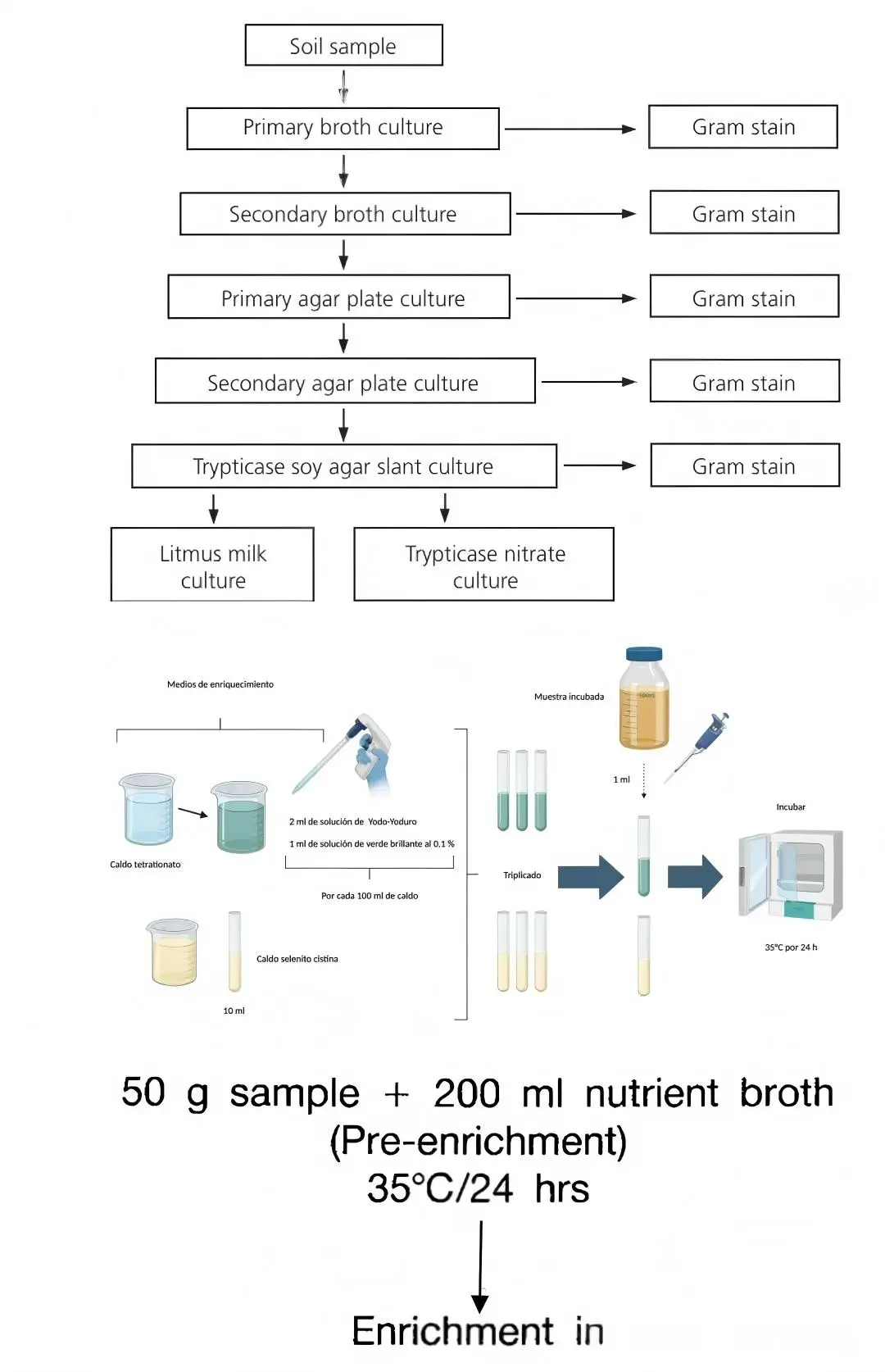
富集培养法是一种基于微生物生理特性的选择性分离方法,其操作流程为,根据目标微生物的生长需求设计选择性培养基,如以特定物质为唯一碳源或氮源、添加特定抑制剂抑制杂菌生长,将待分离样品接入该选择性培养基中,置于适宜条件下培养,使目标微生物在竞争中占据优势并大量增殖,随后将富集后的菌液转接至固体选择性培养基平板,通过划线或涂布法进一步分离纯化。对于专性寄生微生物,则需将样品接种至敏感宿主细胞群体中进行富集培养。
该方法适用于从土壤、水体、临床标本等复杂混合样品中分离含量极低或生长缓慢的特定功能微生物,如降解污染物的菌株、特定病原菌、固氮菌等。其优点是针对性强,能够显著提高目标微生物的分离效率,实现“从混杂群体中精准筛选目标菌株”的目的;缺点是方法设计需基于对目标微生物生理特性的深入了解,富集培养周期较长,且富集产物仍为混合培养物,需结合平板分离技术才能获得纯培养物。
操作注意事项包括,一是选择性培养基的配方需科学合理,确保能有效抑制杂菌生长并促进目标微生物增殖;二是控制适宜的富集培养时间和传代次数,避免目标微生物因过度增殖而衰亡,或因杂菌污染导致富集失败;三是富集后的分离步骤需使用与富集阶段相同或相似的选择性培养基,以维持目标微生物的生长优势。
五)厌氧法
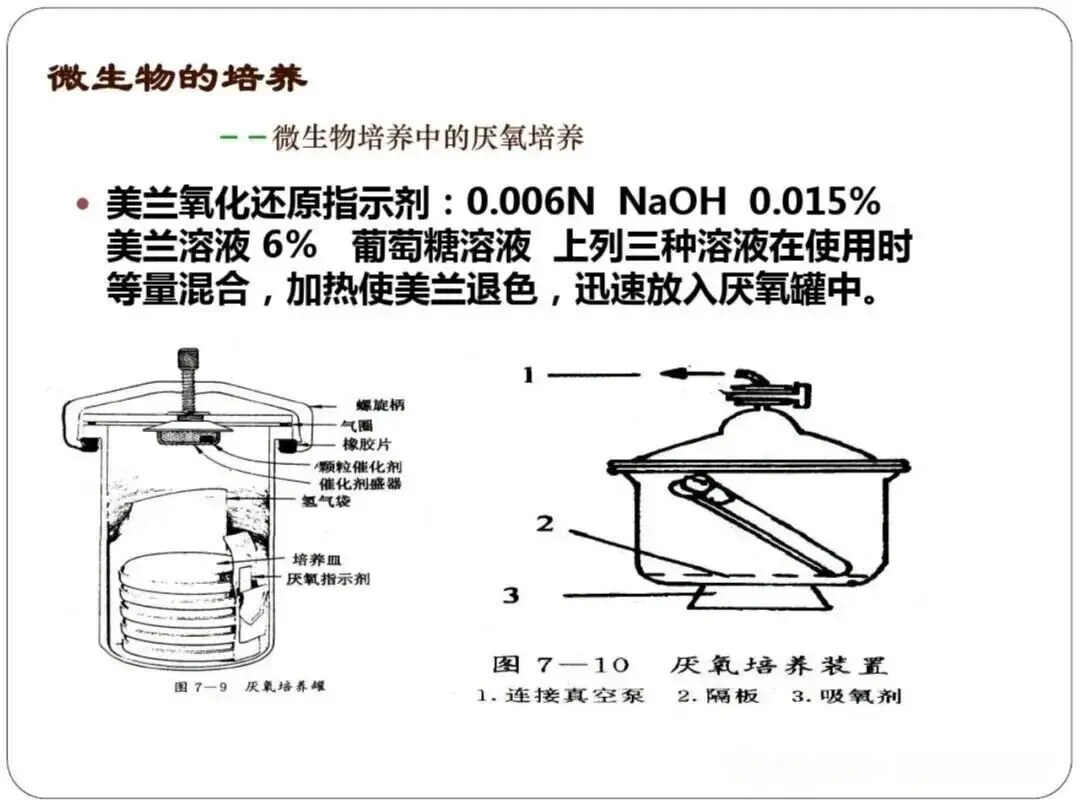
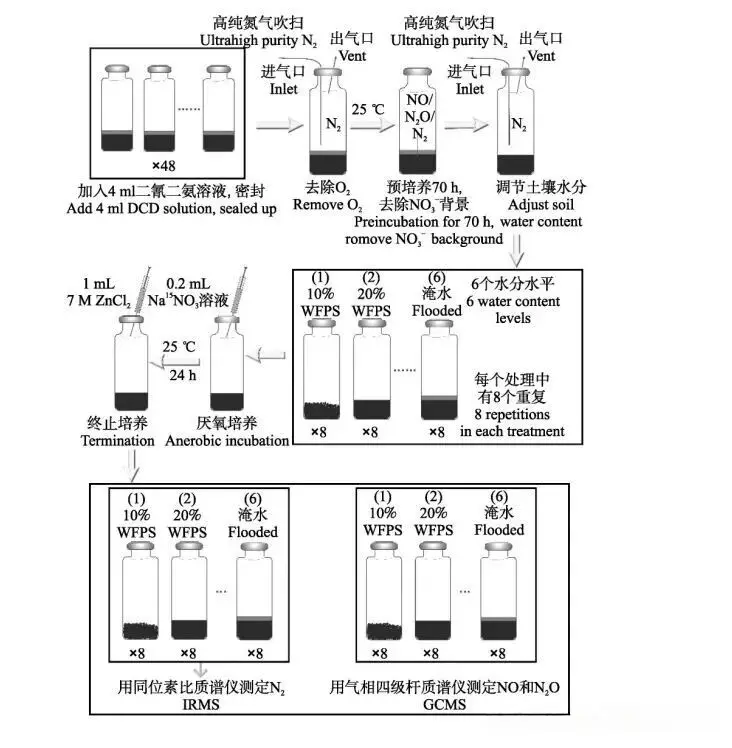
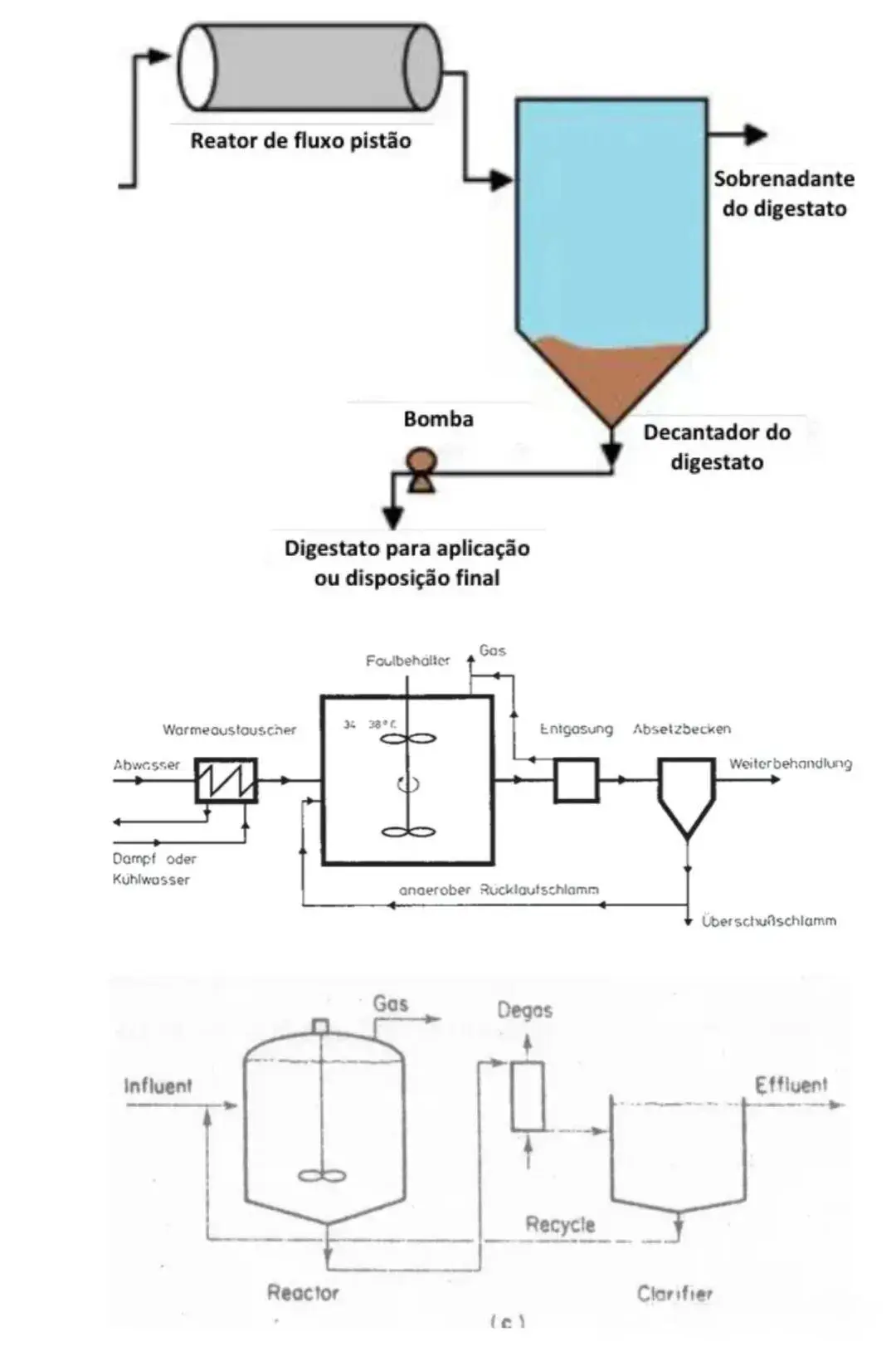
厌氧法是专为分离培养严格厌氧微生物设计的技术,其核心是创造并维持无氧或低氧化还原电位的培养环境,常见操作流程分为三类。第一类为庖肉培养基法,将待分离样品接种至庖肉培养基中,利用培养基中肉渣的还原性物质消耗氧气,同时在培养基表面覆盖无菌液体石蜡或凡士林隔绝空气,随后置于适宜温度下培养;第二类为厌氧罐法,将接种后的平板放入厌氧罐,通过抽真空置换气体或使用产气袋产生氢气与二氧化碳混合气,在钯催化剂作用下将残留氧气转化为水,实现无氧环境;第三类为厌氧工作站法,将整个操作过程置于持续通入氮气、氢气、二氧化碳混合气的全封闭厌氧工作站中完成,确保接种、培养全程无氧气接触。
该方法适用于严格厌氧菌的分离、培养及保藏,如梭菌属、拟杆菌属等常见于肠道、土壤及临床感染样本中的厌氧菌。其优点是能够为严格厌氧菌提供适宜的生长环境,实现此类微生物的有效分离;缺点是操作流程相对复杂,部分方法需专用设备如厌氧罐、厌氧工作站,实验成本较高,且对操作速度要求严格,样品暴露于空气的时间过长会导致厌氧菌死亡。
操作注意事项包括,一是所有培养基和器具需预先进行除氧处理,避免残留氧气影响厌氧菌生长;二是操作过程需迅速高效,最大限度缩短样品与空气的接触时间;三是使用厌氧指示剂如刃天青监测厌氧环境,确保指示剂始终保持无色的无氧状态,定期更换厌氧罐内的催化剂和产气袋,保证厌氧效果稳定。

六)单细胞分离法
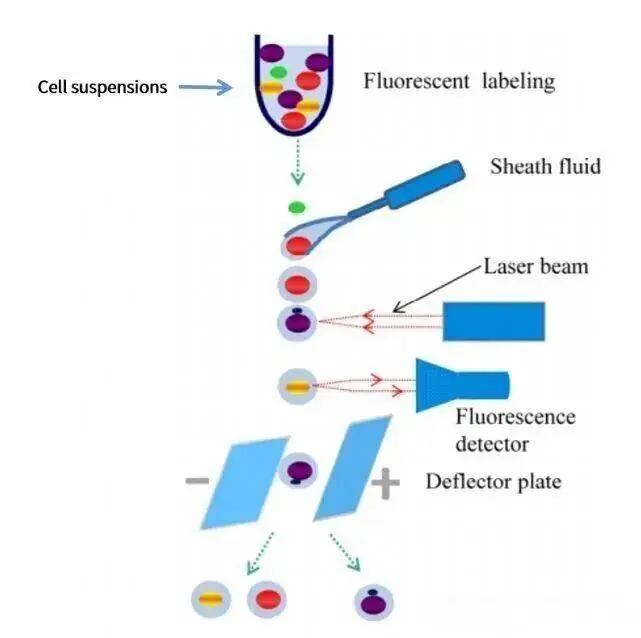
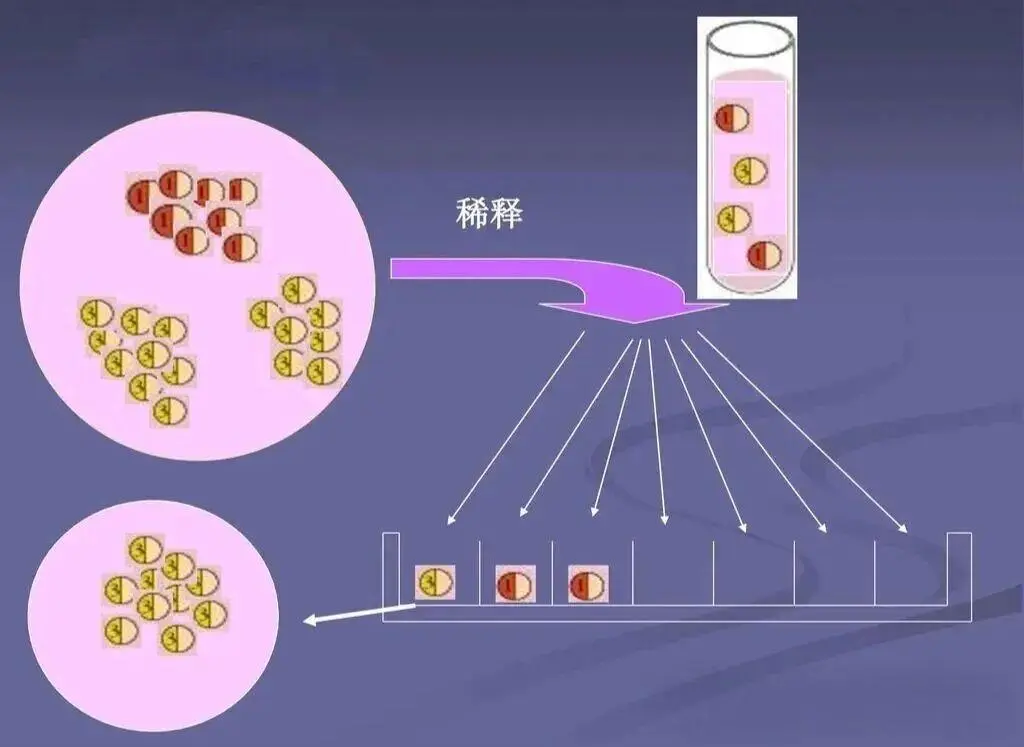
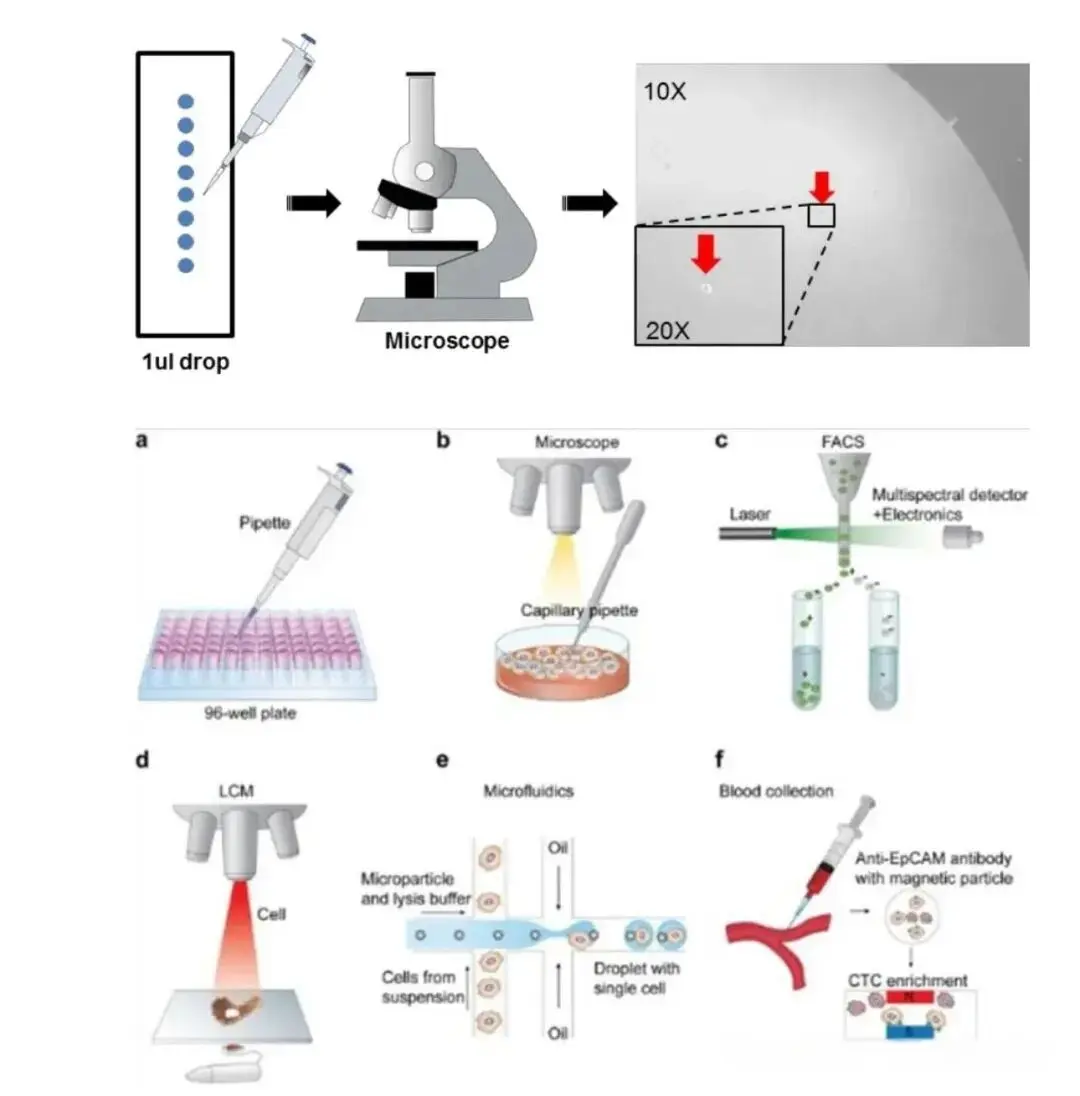
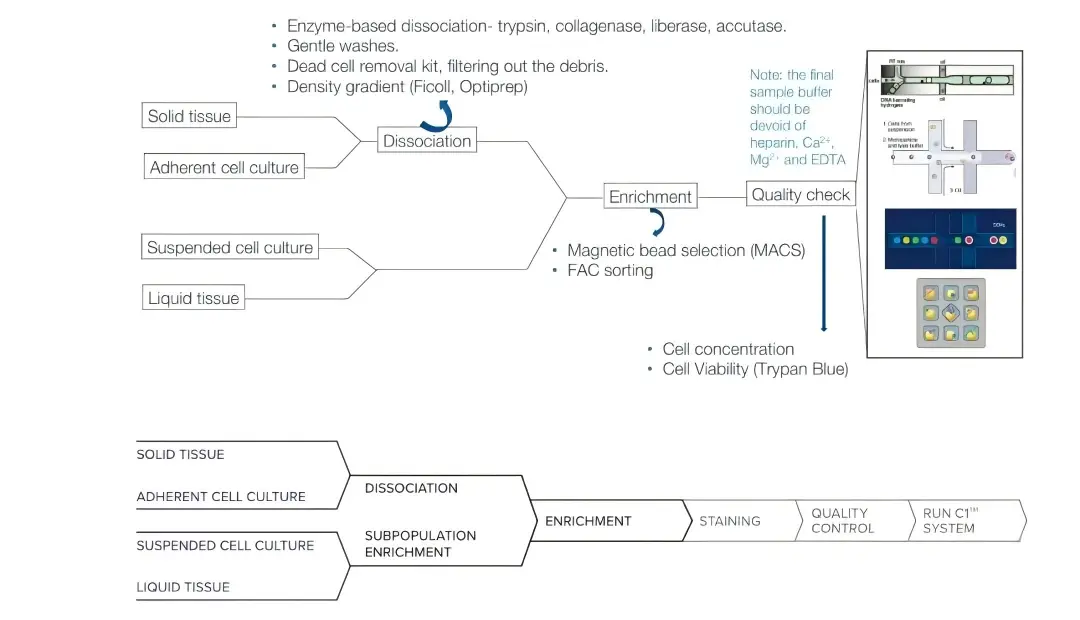
单细胞分离法是一种在显微镜直视下进行的精密分离技术,操作流程需根据微生物个体大小调整。对于个体较大的微生物如真菌孢子、原生动物,可使用显微操作仪操控毛细管直接吸取单个细胞;对于细菌等个体微小的微生物,需借助荧光激活细胞分选仪(FACS),基于细胞的光散射特性和荧光标记实现单细胞分选,或利用微流控技术将细胞悬液包裹于纳升级液滴中,实现单个细胞的精准分离。分离后的单个细胞被转移至适宜的培养基中,置于最佳培养条件下培养,最终获得纯培养物。
该方法适用于分离难以用传统平板法培养的微生物,如不可培养微生物、生长极其缓慢的菌株、细胞间紧密共生的微生物,同时可用于单细胞基因组学、转录组学等前沿研究。其优点是能够实现理论上的绝对纯化,避免传统方法可能存在的微杂菌污染,是研究微生物种群异质性的重要工具;缺点是对仪器设备要求极高,实验成本昂贵,操作技术难度大,需要专业人员进行操作,且除FACS外多数方法的通量较低。
操作注意事项包括,一是样品需制备成均匀的单细胞悬液,避免细胞团块影响分离效果;二是操作环境需保持高度洁净,防止外源污染;三是分离后的单细胞需提供适宜的培养条件,部分微生物可能需要添加生长因子才能生长,同时需通过显微观察验证分离产物为单细胞。
三、各分离纯化技术优缺点与适用范围对比
倾注平板法与涂布平板法均适用于微生物定量计数,前者优势在于定量结果全面,可同时计数表面和深层菌落,后者则胜在菌落形态清晰,便于后续操作。平板划线法操作简便成本低,是日常初步分离的首选方法,但分离效果受人为因素影响较大。富集培养法针对性强,是分离稀有微生物的关键技术,但需结合其他平板方法才能获得纯培养物。厌氧法是分离严格厌氧菌的唯一选择,但操作复杂且需专用设备。单细胞分离法可实现绝对纯化,是前沿研究的重要手段,但仪器成本高、技术门槛高,难以在常规实验室普及。
在实际应用中,常将多种方法组合使用,如先通过富集培养法提高目标微生物的浓度,再使用平板划线法进行分离纯化;对厌氧菌的分离,则需在厌氧环境下结合涂布平板法或划线法完成操作。
四、各国药典对微生物分离纯化的规范要求与异同
一)2025版中国药典的要求
ChP 2025在微生物分离纯化领域的核心要求体现在三个方面。一是强化基于风险评估的微生物控制体系,将分离纯化技术纳入药品全生命周期质量管理,强调从原料、生产环境到终产品的全过程微生物监控;二是规范方法适用性验证,明确要求微生物分离计数方法需通过回收率试验验证,确保供试品中的微生物能够被有效检出,回收率需不低于对照的50%;三是新增不可接受微生物的风险评估与控制指导原则,要求对非无菌产品中分离到的微生物进行鉴定,必要时鉴定至种水平,同时推动微生物全基因组测序等先进技术的应用,提升微生物鉴定的精准性。
二)USP、EP、BP、JP的关键要求
USP在微生物分离纯化方面强调方法的灵活性,如在制药用水微生物检查中,允许使用平皿法或薄膜过滤法,未硬性规定培养基种类,但要求样品尽快检测或冷藏保存,同时在通则<1117>中明确微生物实验室的最佳操作规范,强调第二人复核制度,确保分离计数结果准确可靠。EP与BP的要求高度一致,对培养基配方、培养条件的规定极为具体,如纯化水微生物检查强制使用R2A琼脂培养基,严格限定培养温度和时间,注重方法的可重复性和跨实验室一致性。JP则持续推进与国际药典的协调,其微生物分离纯化相关要求与USP、EP基本接轨,同时保留部分符合日本本土需求的技术细节。
三)各国药典的相同点与不同点
相同点:各国药典均将无菌操作作为微生物分离纯化的核心前提,认可倾注平板法、涂布平板法、平板划线法等经典技术的适用性,强调方法适用性验证的必要性,共同致力于提升微生物检验结果的准确性和可靠性。
不同点:一是培养基与培养条件的差异,ChP与EP推荐使用R2A琼脂进行制药用水微生物检查,USP则未强制规定培养基种类;二是方法灵活性的差异,USP允许根据实际情况选择分离方法,EP和ChP对方法的规定更为严格;三是新增技术接纳程度的差异,ChP 2025积极引入微生物全基因组测序技术,USP和EP则通过增补通则的方式引导快速检测技术的应用。
五、微生物分离纯化的重点难点与风险控制
一)重点难点
微生物分离纯化的核心重点与难点在于确保培养物的纯度与活性。“纯度”要求操作人员具备扎实的无菌操作技能,能够有效避免交叉污染,并通过显微镜检、多次划线传代等手段验证培养物纯度;“活性”则要求深入理解目标微生物的生理特性,精准设计培养基配方和培养条件,尤其对于受损微生物、营养挑剔型微生物,需优化培养基成分如添加生长因子、调整pH值,才能实现其有效分离。此外,从复杂样品中分离特定功能微生物,如何设计科学合理的富集方案,也是技术难点之一。
二)GMP视角下的风险控制
从药品生产质量管理规范(GMP)视角分析,微生物分离纯化过程存在四大风险点。一是交叉污染风险,操作环境消毒不彻底、器具灭菌不充分、操作人员动作不规范等,均可能导致外源微生物污染,控制措施包括严格执行环境监测与消毒规程、强化人员无菌操作培训、定期对无菌器具进行灭菌效果验证;二是假阴性与假阳性风险,抑菌性供试品未被充分中和会导致目标微生物无法生长,选择性培养基特异性不足会导致非目标微生物生长,控制措施包括开展充分的方法适用性验证、使用标准菌株进行阳性对照、优化中和剂的选择与用量;三是厌氧环境失效风险,厌氧罐催化剂失活、密封圈老化会导致氧气渗入,控制措施包括定期更换催化剂和密封圈、使用厌氧指示剂实时监测环境、优化操作流程缩短样品暴露时间;四是数据可靠性风险,记录不完整、菌种编号混乱会导致实验结果无法追溯,控制措施包括建立完善的实验室记录体系、实施菌种统一编号管理、确保实验数据符合ALCOA+原则。
结 语
微生物分离纯化是微生物学领域的基础技术,也是药品微生物质量控制、临床病原学诊断的关键环节。从倾注平板法的温度控制,到平板划线法的手法技巧;从厌氧法的环境营造,到单细胞分离法的精密操作,每一项技术都需要操作人员具备扎实的理论基础和娴熟的实操技能。
2025版《中国药典》及国际主流药典的不断更新,既为微生物分离纯化提供了规范化的操作指南,也对专业人员的技术水平提出了更高要求。在实际工作中,微生物专业人员需熟练掌握各种分离纯化技术的原理与操作要点,深刻理解药典规范的核心要义,强化风险控制意识,将无菌操作贯穿于实验全过程。唯有如此,才能实现“从混杂群体中精准分离目标菌株、获得高纯度纯培养物”的目标,为微生物学研究和药品质量控制提供可靠的技术支撑。
微生物分离纯化技术看似基础,实则蕴含着深刻的科学原理和实践智慧。随着生物技术的不断发展,新的分离纯化技术如微流控技术、单细胞分选技术将不断涌现,但传统平板分离技术的核心地位仍不可替代。夯实基础操作技能,紧跟技术发展趋势,是每一位微生物专业人员的必修课程,也是推动微生物学领域持续发展的根本动力。
参考文献
[1] 中华人民共和国药典委员会.中华人民共和国药典2025年版四部[S].北京:中国医药科技出版社,2025.
[2] United States Pharmacopeial Convention. United States Pharmacopeia 47-National Formulary 42[S]. Rockville: United States Pharmacopeial Convention,2024.
[3] European Directorate for the Quality of Medicines & HealthCare. European Pharmacopoeia 11.0[S]. Strasbourg: Council of Europe,2024.
[4] The British Pharmacopoeia Commission. British Pharmacopoeia 2024[S]. London: The Stationery Office,2024.
[5] 日本药局方编辑委员会.日本药局方第18改正版[S].东京:广川书店,2022.
[6] 周德庆.微生物学教程[M].4版.北京:高等教育出版社,2020.
[7] 范一灵,胡昌勤.2025年版《中国药典》微生物标准的变化与发展趋势[J].中国药品标准,2025,26(01):1-8.
[8] 张军,李琤.药品微生物实验室质量管理规范解读[J].药物分析杂志,2025,45(03):456-463.
[9] 徐威,李雪梅.微生物学实验指导[M].3版.北京:科学出版社,2023.
[10] Cappuccino J G,Sherman N. Microbiology: A Laboratory Manual[M].10th ed. New York: Pearson Education,2021.
本文由环凯转载自“阿郎的银河”公众号,版权归原作者所有,仅供学习参考,如有侵权请联系删除!











