微生物分离与纯化实验——稀释涂布平板法
发布时间:2026-02-05 浏览次数:1346
一、实验目的
通过梯度稀释将混杂微生物样品分散为单个细胞,再经涂布接种在固体培养基表面,形成单菌落(由一个细胞繁殖而来),从而获得纯培养物,用于后续鉴定、保藏或研究。
二、实验原理
梯度稀释:将样品用无菌水/缓冲液进行10倍系列稀释(如10⁻¹、10⁻²、…、10⁻⁶),降低微生物浓度,使单个细胞分散在稀释液中。
涂布分离:取少量稀释液(通常0.1 mL)涂布于固体培养基表面,通过涂布棒的物理分散作用,使微生物均匀分布在培养基上。
单菌落形成:稀释后的单个微生物细胞在适宜条件下繁殖,形成肉眼可见的单菌落(形态一致、孤立分布)。
三、材料与试剂
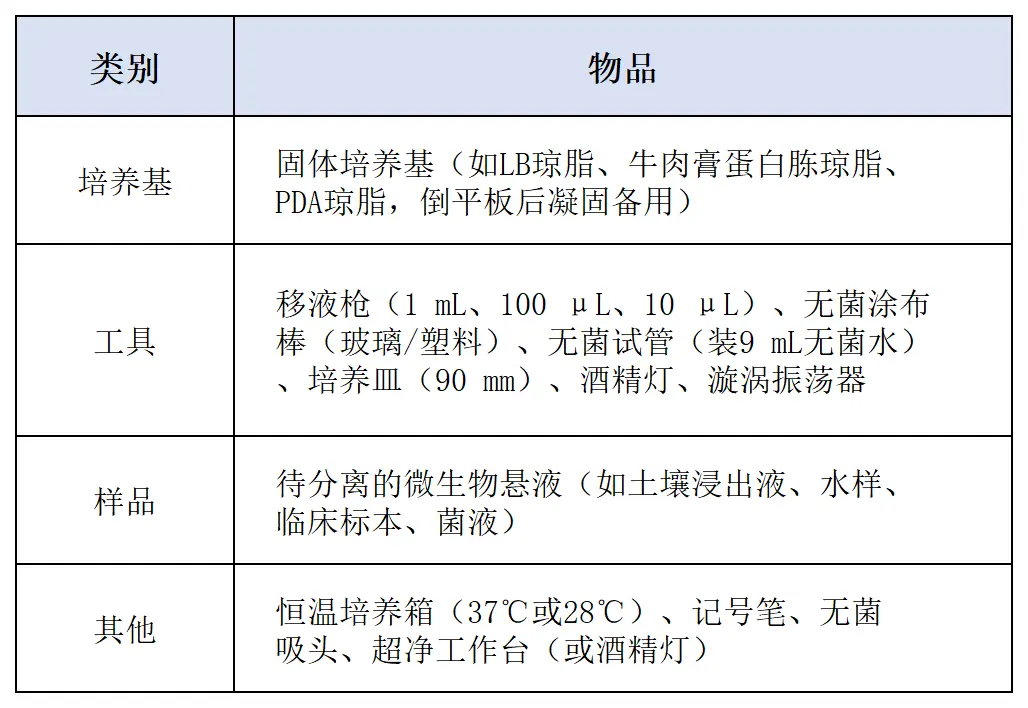
四、操作步骤
1. 准备工作
培养基检查:确保平板无破损、表面干燥(若有冷凝水,倒置平板30分钟晾干)。
标记平板:用记号笔在平板底部标注样品名称、稀释度、日期、操作者(如“土壤菌-10⁻⁴-20260520-张三”),每个稀释度做3个重复平板(减少误差)。
环境消毒:超净工作台开启紫外灯照射10分钟,后用75%乙醇擦拭台面;酒精灯点燃,周围10 cm为无菌区。
2. 样品梯度稀释(10倍系列稀释法)
第一步(10⁻¹稀释):取1 mL待分离样品(如土壤悬液)加入盛有9 mL无菌水的试管中,漩涡振荡器混匀10秒,得到10⁻¹稀释液。
后续稀释(10⁻²~10⁻⁶):用移液枪从10⁻¹稀释液中取1 mL,加入另一支9 mL无菌水试管,混匀得10⁻²稀释液;重复此操作,依次制备10⁻³、10⁻⁴、10⁻⁵、10⁻⁶稀释液(根据样品浓度选择稀释范围,如土壤样品常用10⁻⁴~10⁻⁶,菌液常用10⁻¹~10⁻³)。
3. 涂布平板
取液:用100 μL移液枪从目标稀释度试管中吸取0.1 mL稀释液(若样品浓度极低,可吸取1 mL涂布于大平板)。
涂布操作:打开平板盖(缝隙<1 cm),将稀释液缓慢滴加到培养基表面中央(避免冲击培养基导致凹陷);手持涂布棒(玻璃涂布棒需提前在酒精灯外焰灼烧灭菌,冷却后使用;塑料涂布棒可直接用),将涂布棒轻轻接触培养基表面,以圆周运动均匀涂布稀释液(力度适中,避免划破培养基);涂布完毕后,将平板倒置(防止冷凝水滴落),放入恒温培养箱。
4. 培养与观察
培养条件:
- 细菌:37℃培养18-24小时;
- 真菌(酵母菌/霉菌):28℃培养2-3天;
- 放线菌:28℃培养5-7天(需添加抗生素抑制杂菌)。
结果观察:记录单菌落形态(圆形/不规则、光滑/粗糙、颜色、大小)、数量及分布,选择菌落数30-300个/平板的稀释度进行计数(此为有效计数范围)。
五、结果判断与计算
单菌落标准:孤立、形态一致、直径0.5-3 mm(无重叠)。
活菌数计算(CFU/mL):活菌数=涂布体积(mL)平均菌落数×稀释倍数
示例:10⁻⁴稀释度平板平均菌落数为150个,涂布体积0.1 mL,则活菌数=150×10⁴ / 0.1 = 1.5×10⁷ CFU/mL。
六、注意事项
1.无菌操作核心:
全程在超净工作台或酒精灯旁操作,移液枪枪头、涂布棒需无菌;稀释时试管口、移液枪头避免接触桌面或其他物品。
2.稀释倍数选择:
样品浓度高(如土壤):从10⁻³开始稀释,避免菌落过密;
样品浓度低(如纯菌液):从10⁻¹开始稀释,避免无菌落生长。
3.涂布技巧:
涂布棒需冷却至室温(玻璃涂布棒灼烧后接触培养基边缘试温,无烫痕即可);
涂布速度均匀,确保稀释液覆盖整个培养基表面(边缘留1 cm空白防污染)。
4.培养条件:
倒置培养(防止冷凝水冲散菌落);
厌氧菌需改用厌氧平板,在厌氧罐中培养(含催化剂除氧)。
七、常见问题与解决方法
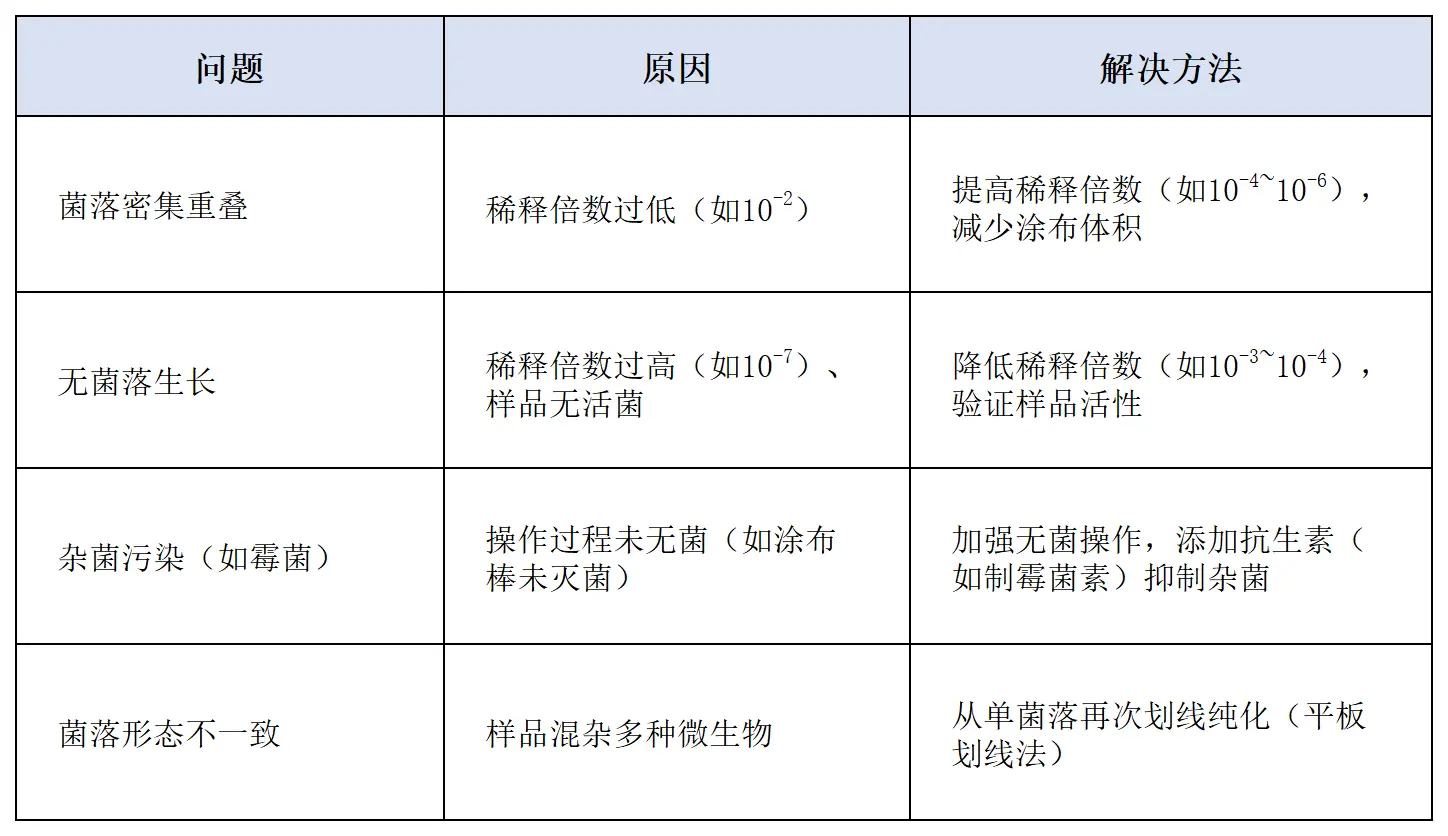
八、总结
稀释涂布平板法是微生物分离的“金标准”,核心是梯度稀释+均匀涂布,通过控制稀释倍数和涂布操作获得单菌落。该方法适用于好氧微生物的分离,且可通过菌落计数量化样品中活菌数量。熟练后可根据样品特性调整稀释范围和涂布体积,提高分离效率。
附:操作流程简图
样品→10⁻¹稀释(1 mL样+9 mL水)→10⁻²~10⁻⁶稀释→取0.1 mL稀释液涂布平板→倒置培养→观察单菌落→计数/纯化。
本文由环凯转载自“普西唐阮杭”公众号,版权归原作者(阮杭)所有,仅供学习参考,如有侵权请联系删除!











