标准菌株反复冻融的风险与规范化管理指南!
发布时间:2026-02-12 浏览次数:212
标准菌株是微生物检测、方法验证、质量控制及科研工作的“基准尺”,其遗传稳定性、生理活性和纯度直接关系到实验结果的可靠性。因此,反复冻融(即多次冷冻-解冻)对标准菌株的影响不容忽视,必须通过科学规范的管理加以规避。
一、反复冻融对标准菌株的主要负面影响
1. 细胞结构损伤与存活率显著下降
冰晶形成:冷冻过程中胞内外水分结晶,刺穿细胞膜/壁,导致内容物泄漏。
渗透压冲击:解冻时水分快速进入细胞,造成膨胀破裂;或脱水导致代谢停滞。
敏感菌株尤甚:如乳酸菌、双歧杆菌、厌氧菌、奈瑟氏菌等,1–2次冻融即可损失50%以上活菌数。
2. 遗传物质不稳定,表型漂变
冻融过程诱发氧化应激,产生自由基,损伤DNA。
可能导致:
基因突变或缺失
质粒丢失(影响抗性、产酶等特性)
表型改变(如生化反应异常、生长速率下降)长期反复操作将使菌株偏离原始标准特性,丧失“标准”意义。
3. 污染与交叉污染风险升高
每次取用均需开盖操作,增加环境微生物、气溶胶或操作者带入杂菌的风险。
若未严格分区操作,不同菌株间可能发生交叉污染,导致鉴定错误。
4. 功能活性退化
关键酶(如β-半乳糖苷酶、过氧化氢酶)活性下降。
代谢产物(如有机酸、细菌素)合成能力减弱。
对于用于抗生素效价测定或药敏试验的菌株,可能导致假阴性或MIC偏移。
二、标准菌株规范管理的核心措施
1. “一次性分装”原则
初次复苏后,将菌悬液与保护剂(如20%甘油)等体积混合。
分装至0.5–1 mL/管的无菌冻存管中。
每管仅使用一次,严禁“用不完再冻回”。
2. 选择适宜的冻存条件
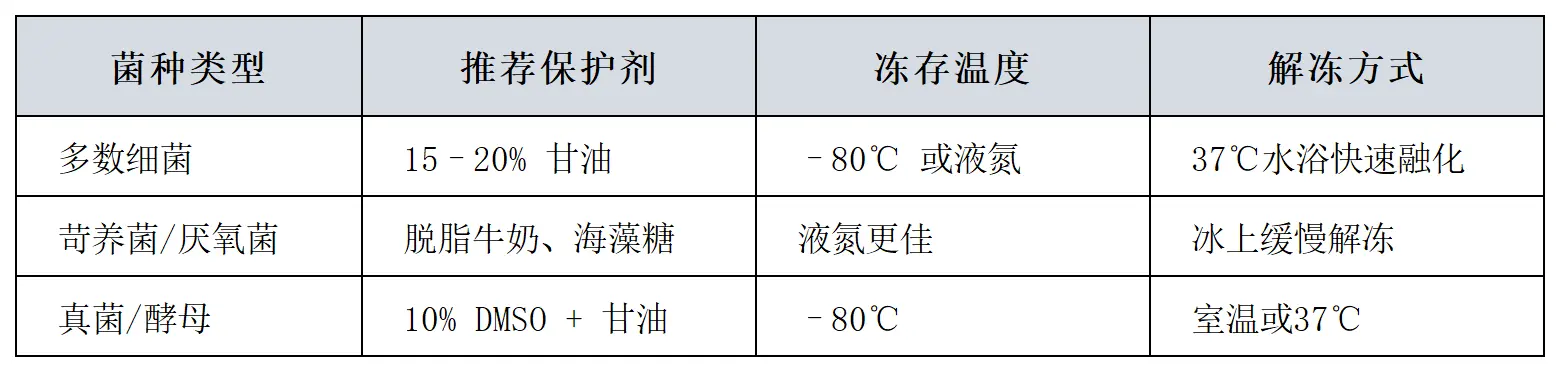
3. 建立三级菌种库体系
主种子批(Master Seed Lot):原始标准菌株,永不直接使用,仅用于制备工作种子。
工作种子批(Working Seed Lot):由主种子批传代1–2次后分装,用于日常实验。
使用级菌液:由工作种子批当日制备,当日用完,不保存。
4. 严格记录与可追溯性
每支冻存管标签应包含:
菌株名称与编号(如ATCC 25922)
冻存日期与代次(P1, P2…)
操作人、保护剂类型
累计冻融次数(建议在电子台账中记录)
5. 定期复核与报废机制
每6–12个月对库存菌株进行复苏验证:
形态(革兰染色、镜检)
纯度(划线无杂菌)
生化特性(如API鉴定)
功能验证(如药敏、产酸)若出现特性偏离、活力下降或污染,立即隔离并报废。
三、权威依据与行业共识
《中国药典》2020年版:明确要求标准菌株应“避免反复冻融”,建议采用“小量分装、单次使用”。
ISO/IEC 17025:强调标准物质(含菌株)的稳定性监控与使用控制。
CLSI M22-A3:指出反复冻融可能导致药敏质控菌株MIC漂移,影响质控结果判断。
ATCC官方指南:建议用户收到冻干粉后,自行扩增并分装至少20管以上,以减少主库存使用频率。
通过科学分装、严格操作、规范记录和定期验证,可最大限度避免反复冻融带来的风险,确保标准菌株在检测、科研和生产中持续发挥“金标准”作用。
文章来源于网络,版权归原作者所有,仅供学习参考,如有侵权请联系删除!






