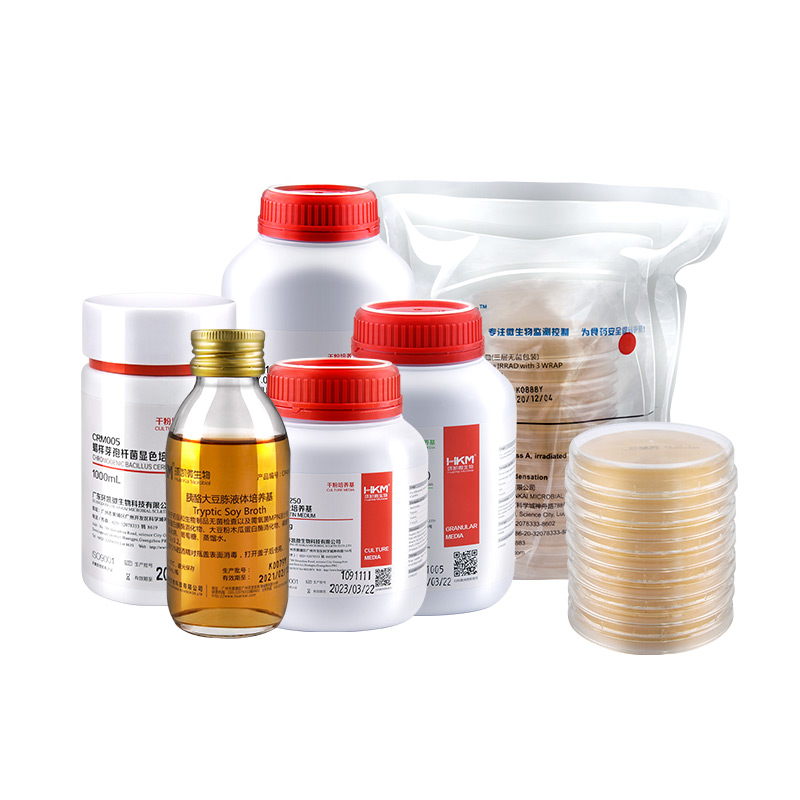
2025年版GB/T 16293浮游菌标准学习
发布时间:2026-04-10 浏览次数:513
GB/T 16293-2025《医药工业洁净室(区)浮游菌的测试方法》,与GB/T16293-2010相比,主要变化如下:
一、 增加了浮游菌采样器工作原理
标准描述了一般采用的筛孔式撞击采样器的原理,并明确提出了应定期对采样器进行校准的要求。
讨论:了解设备的工作原理无疑是有益的。然而,新版标准并未给出采样器校准的具体标准。经查询,国内外存在多种相关的校准标准,测试项目繁多且要求各异。基于此,笔者的理解是:既然新版GB/T 16293-2025未规定具体校准规程,那么在合规性层面上,只要执行了校准并保留了完整的校准记录自圆其说即可。
二、 增加了培养基的要求
标准要求培养基的管理及适用性检查应符合《中国药典2025年版四部》9203的相关规定。但在培养计数部分,其培养条件与药典的规定有所不同,明确提出“宜根据环境污染微生物历史数据及种群特性调整培养方案”。
具体培养方案包括:
仅使用TSA时:可采用20℃~25℃培养3d~5d后,再转移至30℃~35℃培养2d~3d;或先在30℃~35℃培养2d~3d后,再转移至20℃~25℃培养3d~5d。
增加SDA时:在20℃~25℃培养5d~7d。
讨论:在确定具体培养方案前,首要工作是了解环境的污染微生物历史数据。应根据历史数据中优势微生物的种类(偏向细菌或真菌),优先选择其最适温度条件进行培养。据了解,部分第三方检测机构早已在沉降菌或浮游菌的检测报告中区分并标注细菌与真菌的计数结果。尽管此类菌落鉴定数据可能不完全精确(例如未进一步区分酵母菌),但这可被视为应对新要求的提前准备。若无历史数据,则需从现在开始创造历史。
反思: 原有的培养条件既然已能收集到这些微生物,按照培养结果去推导培养条件并更换培养条件,其效果是否会更好,也犹未可知。
三、 测试条件
标准规定:
洁净室(区)确认时:应在静态和动态两种占用状态下进行测试。
洁净室(区)常规监测时:应在动态条件下进行测试。
静态测试自净时间:单向流洁净室不少于10分钟,非单向流洁净室不少于30分钟。
讨论:标准中使用的“洁净室(区)确认”一词,笔者认为在行业惯例中称为“验证”更为贴切。在进行新建洁净室验证时,相应的静态与动态测试项目、采样点及验收标准应在验证方案中予以明确规定。例如,在药品GMP中只规定了浮游菌的动态标准;而在GB 17405-2025《保健食品良好生产规范》中,则对动态和静态均有要求。如果有其他行业标准也有规定,欢迎留言补充。
表1:GB 17405-2025 浮游菌要求
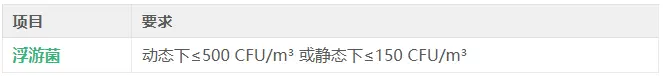
关于“监测应在动态条件下进行”,此“动态条件”需要进一步细化。对于药品微生物实验室,其浮游菌的监测频率和动态标准可直接参考《中国药典2025年版四部》9205的要求。
表2:《中国药典》2025年版四部 9205 微生物实验室环境监测频次要求
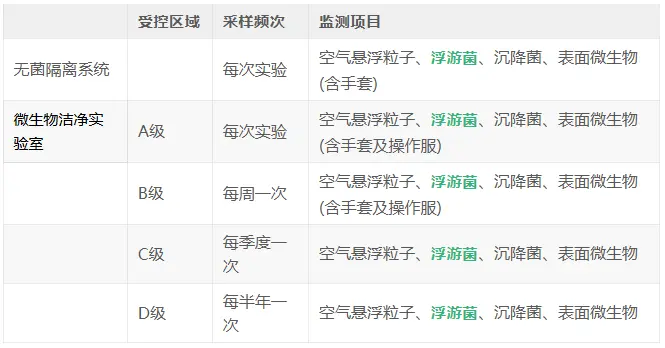
表3:《中国药典》2025年版四部 9205 洁净区微生物监测动态标准
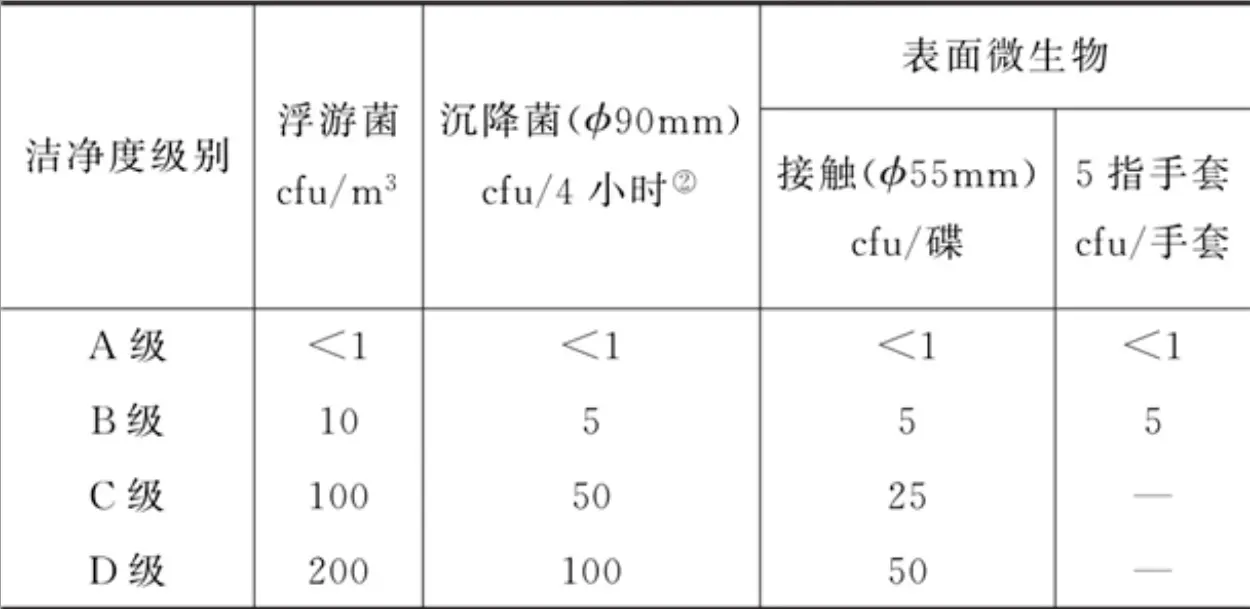
需注意,不同洁净级别的监测目的有所侧重:A级环境的监测重在收集可能存在的污染微生物,用于后续的污染调查;而B、C、D级环境的监测则重在通过数量监测环境的趋势变化。
四、 更改了采样点的要求
标准要求,洁净室(区)在确认及监测时,应基于风险评估确定采样点的数目及位置(包括水平和垂直位置)。同时强调,通过风险评估确定的采样点布置,还必须满足标准中表1规定的最少采样点数目要求。
讨论:此要求与悬浮粒子的采样点布点思路有所不同。采样点的确定需要在满足“最少采样点”这个最低硬件要求的基础上,再通过风险评估进行增加或优化。从操作便利性角度考虑,建议将风险评估识别出的关键采样点,尽可能地整合到满足最少点数要求的布点方案中,以提高监测效率。
五、 增加了不同洁净级别的最小采样量要求
标准根据洁净级别和测试状态(静态/动态),明确了最小采样量,并由此指导设置采样时间。
讨论:标准中要求对阴性对照进行“同法操作”,这部分主要考量的是培养皿在移动、搬运过程中可能引入污染的风险。然而,如果使用的是商业化的、灭菌包装的预制培养基平板,那么此操作更多考验的是预制培养基产品本身的灭菌保证水平及其包装的完整性。
本文由环凯转载自“石决明”公众号,版权归原作者所有,仅供学习参考,如有侵权请联系删除!