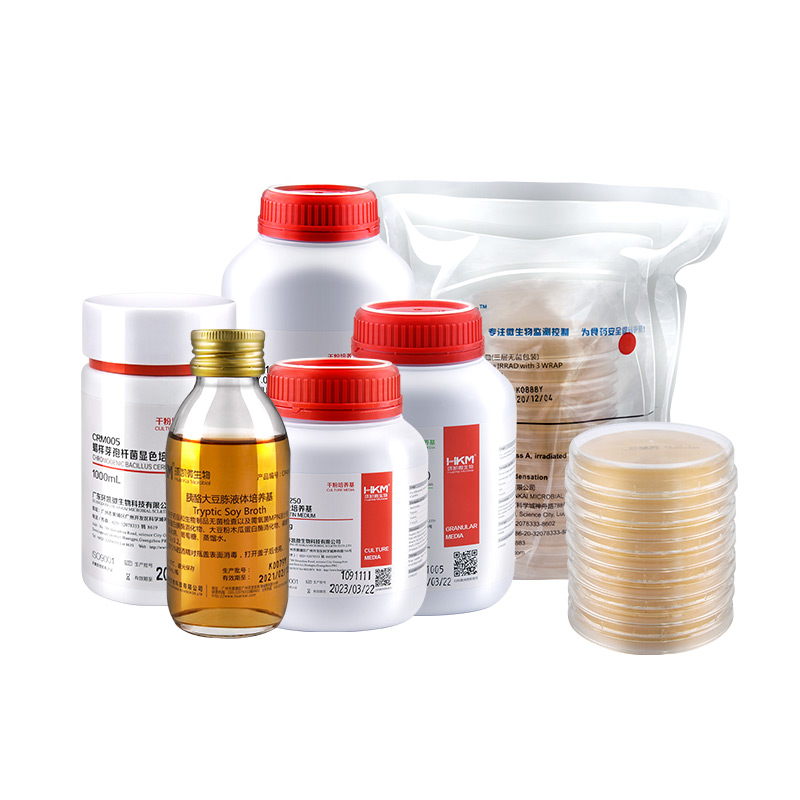
沉降菌皿(培养基碟)验证方案
发布时间:2026-04-22 浏览次数:297
1. 验证目的
确认沉降菌皿(含培养基)的设计、制备/采购、性能符合既定标准及药典要求,确保其能够有效捕获、促进并支持空气中微生物的生长,为洁净区的环境监测提供可靠数据。
2. 适用范围
本方案适用于环境监测中使用的各类沉降菌皿,包括:
实验室自制的沉降菌皿(干热/湿热灭菌后灌装培养基)
商业化即用型沉降菌皿(经辐照灭菌的成品培养基)
常用培养基类型:胰酪大豆胨琼脂(TSA)、沙氏葡萄糖琼脂(SDA)等
3. 验证依据
《药品生产质量管理规范》(GMP)2010版 附录1 无菌药品
《中国药典》四部 1105 微生物计数法
《中国药典》四部 9205 药品洁净实验室微生物监测和控制指导原则
ISO 14698 洁净室及相关受控环境——生物污染控制
GB/T 16294 医药工业洁净室(区)沉降菌的测试方法
培养基生产商的质量标准
4. 验证小组与职责
职务 | 姓名 | 职责 |
|---|---|---|
| 验证主管 | XXX | 审核验证方案及最终报告,批准验证结论。 |
| 微生物/环境监测负责人 | XXX | 执行验证测试,准备菌种,收集数据,撰写报告。 |
| QA(质量保证) | XXX | 监督验证过程,审核原始数据及报告。 |
| 采购/物料管理 | XXX | 负责商业化皿的采购、验收和存储管理。 |
5. 验证内容
5.1 设计确认 (DQ)
5.1.1 目的:确认沉降菌皿的设计、材质及培养基选择符合用户需求标准(URS)。
5.1.2 内容:
- 确认培养皿尺寸(通常为 90mm×15mm)符合标准采样器/培养要求。
- 确认培养基类型(TSA用于细菌,SDA用于霉菌和酵母菌)是否匹配监测需求。
- 确认皿的材质(聚苯乙烯)是否无菌、透明、无抑制微生物生长的物质。
- 确认包装方式(单层/双层无菌包装)是否满足进入不同洁净区的需求。
5.2 安装/接收确认 (IQ)
对于商业化即用型沉降菌皿,这一步是入库验收;对于自制皿,是制备过程确认。
5.2.1 商业化即用型皿的接收确认
5.2.1.1 外观检查:
- 包装完好,无破损、无污染。
- 培养皿无裂痕,培养基无干裂、无气泡、无析出、无污染迹象。
5.2.1.2 信息核对:
- 核对产品名称、批号、有效期、储存条件与采购订单/COA一致。
- 检查供应商提供的合格证书(COA) 是否齐全,促生长试验结果是否合格。
5.2.1.3 储存条件确认:确认运输和储存温度是否符合要求(通常 2-25℃ 避光)。
5.2.2 自制皿的制备确认
培养基配制:确认培养基配方、称量、溶解、灭菌(121℃ 15分钟)过程符合SOP。
环境控制:确认灌装操作在洁净工作台或A级层流下进行。
灌装量:确认每皿灌装量(通常 15-20 ml),使培养基厚度均匀(约 4-5 mm)。
包装:确认凝固后放入原包装袋或无菌袋中密封,标明名称、批号、制备日期。
5.3 运行/性能确认 (OQ/PQ)
这是验证的核心,必须按照《中国药典》1105的要求进行培养基的适用性检查。
5.3.1 无菌性检查
5.3.1 .1 目的:确认沉降菌皿本身是无菌的,无背景污染。
5.3.1 .2 方法:
- TSA 皿:30-35℃ 培养 3-5 天。
- SDA 皿:20-25℃ 培养 5-7 天。
- 从每批制备/采购的沉降菌皿中,随机抽取一定数量(通常为 5-10 个,或总盒数的 1%)。
- 将抽出的沉降菌皿直接放入培养箱中培养:
5.3.1 .3 合格标准:所有抽检皿培养后应无菌生长。若发现有菌生长,需启动偏差调查,该批次可能需报废处理。
5.3.2 促生长能力检查(灵敏度测试)
5.3.2.1 目的:确认培养基能够支持目标微生物的生长(这是最关键的性能指标)。
5.3.2.2 测试菌株(根据培养基类型选择):
- 白色念珠菌(Candida albicans) CMCC(F) 98001
- 黑曲霉(Aspergillus niger) CMCC(F) 98003
- 金黄色葡萄球菌(Staphylococcus aureus) CMCC(B) 26003
- 铜绿假单胞菌(Pseudomonas aeruginosa) CMCC(B) 10104
- 枯草芽孢杆菌(Bacillus subtilis) CMCC(B) 63501
- TSA 皿(用于细菌):
- SDA 皿(用于霉菌和酵母菌):
5.3.2.3 方法:
制备菌悬液:将各标准菌株新鲜培养物制成浓度约为 10² CFU/ml 的菌悬液(每皿最终接种量应 < 100 CFU)。
接种:取 3 个待测沉降菌皿,每个皿表面滴加 0.1 ml 菌悬液,用无菌涂布棒涂布均匀。每种菌株分别做 3 个平行皿。
设立对照:使用经批签发的对照培养基(或已验证合格的批次)同步进行涂布接种,作为阳性对照。
培养:按规定的温度和时间培养。
计数:培养后计算各平皿的菌落数。
5.3.2.4 合格标准:待测培养基上的菌落数应不小于对照培养基上菌落数的 70%,且菌落形态应典型、生长良好。
5.3.3 抑菌性检查(可选/针对特定环境)
5.3.3.1 目的:确认如果环境中存在消毒剂残留,皿中的培养基不会因此产生抑菌性(通常用于清洁验证后的环境监测评估)。
5.3.3.2 方法:
- 在待测沉降菌皿表面涂布一定量的常见消毒剂残留液(如低浓度过氧化氢、季铵盐等)。
- 然后进行 5.3.2 促生长能力检查,与未经消毒剂处理的对照皿比较菌落生长情况。
5.3.3.3 合格标准:消毒剂处理后,菌落回收率应 ≥ 70%(相对于对照),否则说明环境监测时需考虑消毒剂中和剂的使用。
5.3.4 储存有效期验证
5.3.4.1 目的:确认沉降菌皿在规定的储存条件下,在其标称的有效期内性能保持稳定。
5.3.4.2 方法:
- 在制备/采购后(0个月)、中期(如1.5个月)、末期(有效期终点,如3个月),分别抽取样品。
- 在每个时间点,重复 5.3.1 无菌性检查 和 5.3.2 促生长能力检查。
5.3.4.3 合格标准:在整个有效期内,所有时间点的无菌性和促生长能力均应符合标准。如果末期不合格,需缩短有效期。
6. 环境监测模拟(可选/应用确认)
目的:在实际监测场景下(如A级区气流下),确认皿的放置和暴露不会引入污染。
方法:
- 在洁净室模拟日常监测,打开沉降菌皿盖,暴露规定时间(如4小时)。
- 盖好皿盖,按标准培养。
- 同时设置阴性对照(不开盖的皿)和阳性对照(人工加菌的皿)。
合格标准:暴露后的沉降菌皿应无菌生长或符合该区域动态标准;阴性对照应无菌生长;阳性对照应生长良好。
7. 可接受标准汇总
无菌性:抽检皿培养后无菌生长。
促生长能力:待测皿上的菌落数 ≥ 对照皿菌落数的 70%。
有效期:在有效期内性能保持稳定。
物理特性:包装完整,培养基无干裂、无污染。
8. 再验证/批次放行
沉降菌皿属于消耗品,需要每批次进行放行测试:
商业化即用型皿:每接收一批新批号,均需进行无菌性检查和促生长能力检查,合格后方可放行用于环境监测。
自制皿:每制备一批,均需进行上述两项检查。
对于供应商审计合格、历史数据稳定的商业化产品,可适当降低抽检频率(如每3批抽检1批),但首次使用或变更供应商时必须全检。
9. 验证结果与结论
验证报告需汇总该批次的测试数据(无菌培养记录、各菌株计数结果),得出结论:本批次沉降菌皿的各项性能指标符合药典及GMP要求,验证合格,可用于洁净区的沉降菌监测。
常见注意事项(验证失败原因排查)
1,无菌性不合格(有污染):
- 自制皿:灌装环境不达标、灭菌不彻底、操作污染。
- 商业化皿:包装破损、辐照灭菌失败、运输储存不当。
2,促生长能力不合格(菌长得不好):
- 培养基配制不当(pH值不准、过度加热)。
- 培养基原料质量问题。
- 储存条件不当(过热、冷冻、光照导致培养基变质)。
- 菌种老化或制备的菌悬液浓度不准。
3,培养基干裂/萎缩:
- 灌装量不足。
- 储存时间过长,水分蒸发(包装密封性不好)。
- 储存环境过于干燥。
4,菌落蔓延:
- 涂布时未将菌液完全涂干。
- 皿盖有冷凝水滴落。
5,计数困难:培养基有气泡,干扰菌落观察。
本文由环凯转载自转载自“器械姬”公众号,版权归原作者所有,仅供学习参考,如有侵权请联系删除!