制药无菌工艺验证必备:培养基模拟灌装(MFT)全解析与合规指南
发布时间:2026-04-17 浏览次数:1141
一、引言:一个让质量负责人夜不能寐的问题
想象一下:你是一家无菌制剂企业的质量负责人,明天就要迎接药监局的GMP检查。
检察官问:"你们如何证明过去半年生产的这500万支注射液是无菌的?"
你深吸一口气,递上厚厚一沓资料:培养基模拟灌装试验(Aseptic Process Simulation)报告。
这不是一份普通的验证报告——它是制药企业无菌工艺能力的"体检报告",是每一次药品放行前必须通过的"期末考试",更是GMP法规明确要求的必检项目。
核心认知:没有一份合格的培养基模拟灌装报告,任何无菌产品都不能上市。这就是培养基模拟灌装的分量。
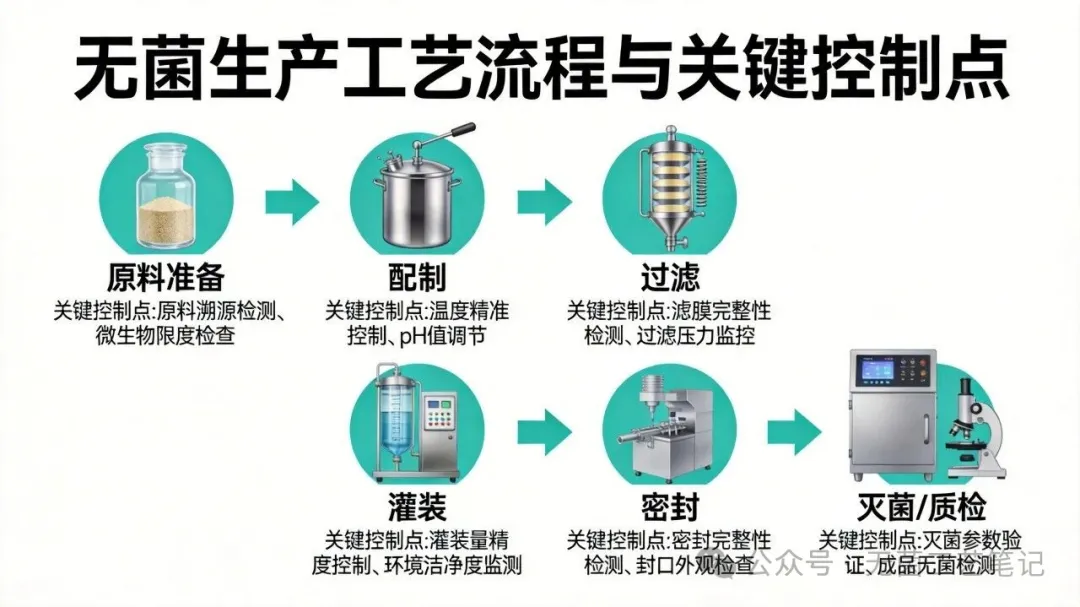
二、核心概念:什么是培养基模拟灌装?
2.1 定义与原理
培养基模拟灌装(Media Fill / Aseptic Process Simulation,MFT),是指采用微生物生长支持性培养基替代实际产品,完全模拟无菌生产全流程操作、环境条件、人员干预,通过培养后样品的微生物检出情况来评估无菌工艺可靠性的验证活动。
用一个通俗的比喻:就像消防演习,用"假火"检验灭火系统是否有效。培养基模拟灌装用"培养基"替代"药品",用"模拟污染"检验"无菌工艺"是否可靠。
核心逻辑:
✅ 如果无菌工艺有效 → 培养基保持无菌 → 无微生物生长 → 通过
❌ 如果无菌工艺有漏洞 → 培养基被污染 → 微生物生长 → 失败
2.2 适用范围
培养基模拟灌装适用于所有非最终灭菌的无菌产品生产,包括但不限于:
产品类型 | 包装形式 |
|---|---|
小容量注射剂 | 安瓿、西林瓶 |
注射用冻干制剂 | 西林瓶 |
预充式注射器 | 预充针、卡式瓶 |
生物制品 | 西林瓶、输液袋 |
细胞与基因治疗产品 | 冻存管、注射器 |
BFS(吹灌封)产品 | 塑料安瓿 |
重要提示:采用最终灭菌工艺(如湿热灭菌、辐射灭菌)生产的产品不需要培养基模拟灌装,因为产品在密封后经过灭菌处理,无菌保证由灭菌工艺本身保障。
三、法规要求:GMP、PDA TR、国际指南
3.1 中国GMP(2023年修订)附录1要求
根据《药品生产质量管理规范(2023年修订)》附录1 无菌药品,核心要求如下:
第四十七条:无菌生产工艺的验证应当包括培养基模拟灌装试验。
应当根据产品的剂型、培养基的选择性、澄清度、浓度和灭菌的适用性选择培养基。应当尽可能模拟常规的无菌生产工艺,包括所有对无菌结果有影响的关键操作,及生产中可能出现的各种干预和最差条件。
批次规模与合格标准
灌装数量 | 污染阳性标准 |
|---|---|
< 5000支 | 不得检出任何污染品(零容忍) |
5000-10000支 | 1支污染→调查后可重试;2支污染→调查后重新验证 |
> 10000支 | 1支污染→调查;2支污染→调查后重新验证 |
试验频率
首次验证:每班次连续进行3次合格试验
定期再验证:每班次每半年至少1次,每次至少一批
变更后验证:空气净化系统、设备、生产工艺及人员重大变更后需重复试验
3.2 国际指南对照
法规/指南 | 核心要求 |
|---|---|
EU GMP Annex 1(2022版) | 强调污染控制策略(CCS),要求最差条件验证 |
FDA Aseptic Processing Guidelines | 批次规模≥5000-10000支,明确干预模拟要求 |
PDA TR 47 | 详细实施指南,覆盖干预分类、批次规模、环境监测 |
ISO 13408-1:2022 | 医疗保健产品无菌加工通用要求 |
WHO TRS 961 Annex 6 | 国际药品认证合作组织要求 |
法规要点速查:
首次验证:每班次连续3次合格
再验证频率:每半年1次/班次
最小样本量:≥3000支
合格标准:<5000支→零污染;≥5000支→污染率≤0.1%
目标:零污染(Zero Contamination)
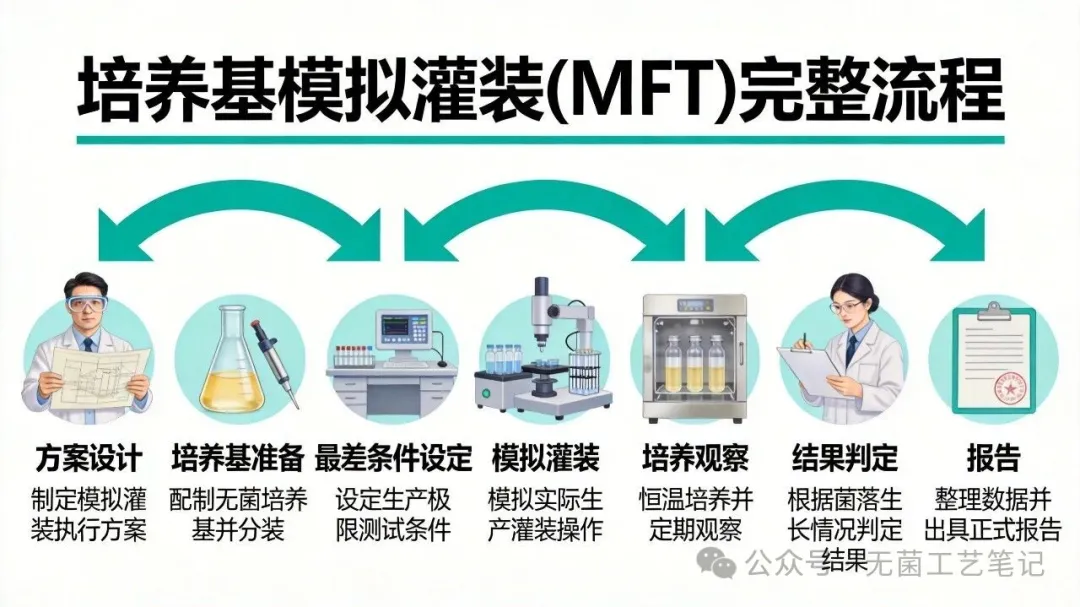
四、实施要点:如何设计和执行一次合格的MFT
4.1 试验方案设计
培养基选择:
培养基类型 | 适用场景 | 验证要求 |
|---|---|---|
| TSB | 需氧菌、真菌培养首选 | pH值与产品偏差≤±0.5 |
| FTM | 厌氧菌易感剂型 | 需氧+厌氧双条件培养 |
促生长试验验证:每批次培养基使用前必须完成促生长试验,接种标准菌株。
菌种 | 接种量 | 培养温度 |
|---|---|---|
金黄色葡萄球菌 CMCC(B)26003 | ≤100CFU | 30-35℃ |
铜绿假单胞菌 CMCC(B)10104 | ≤100CFU | 30-35℃ |
枯草芽孢杆菌 CMCC(B)63501 | ≤100CFU | 30-35℃ |
白色念珠菌 CMCC(F)98001 | ≤100CFU | 20-25℃ |
黑曲霉 CMCC(F)98003 | ≤100CFU | 20-25℃ |
合格标准:各菌株生长率≥对照培养基的70%
4.2 最差条件设定
⭐ 这是培养基模拟灌装最核心的设计原则:必须覆盖所有可能的高风险场景!
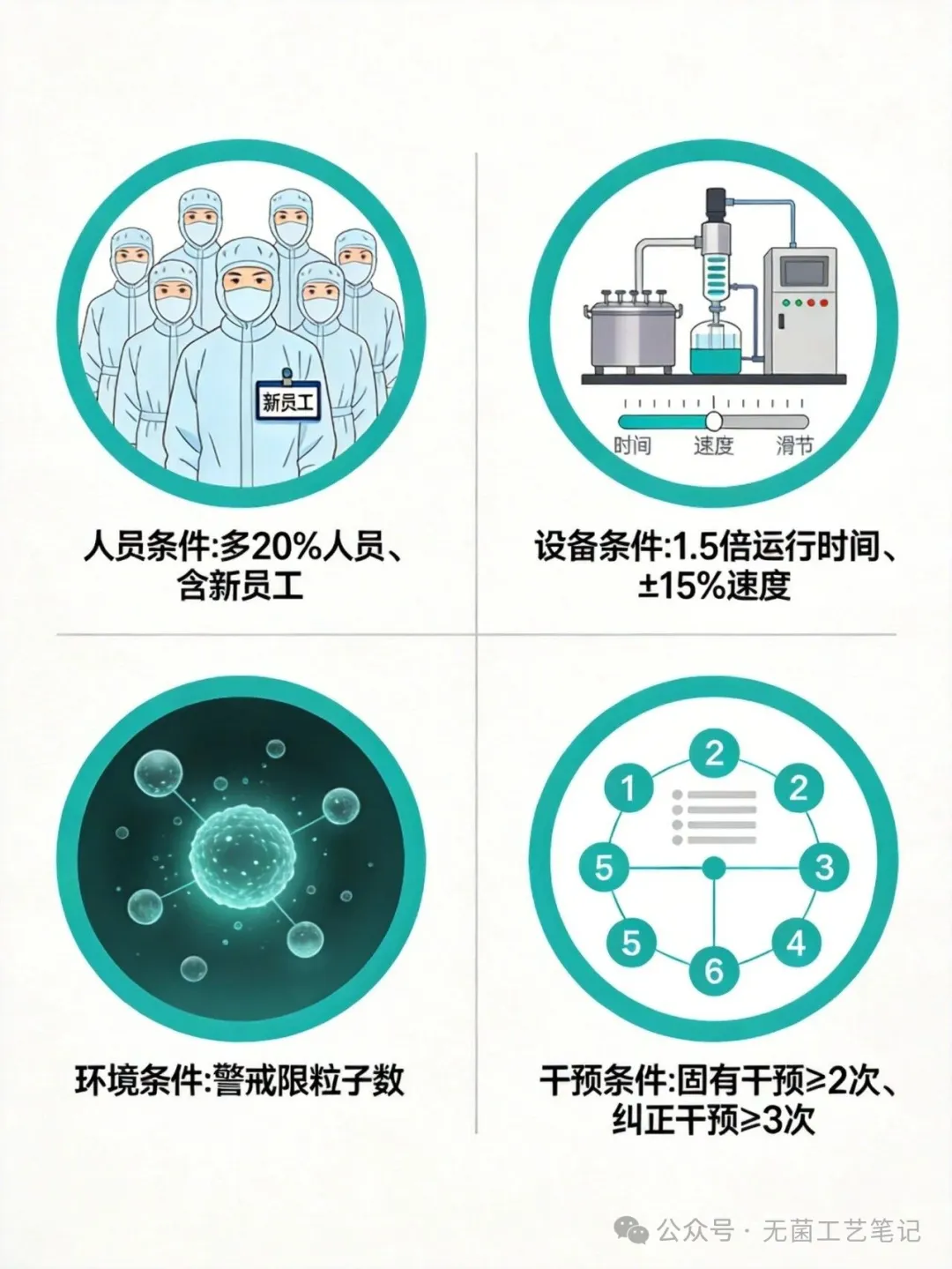
1、人员条件:作业人员数量较正常生产多20%;至少包含1名入职不满3个月的新员工
2、设备条件:生产线运行时间为正常批次的1.5倍;灌装速度覆盖额定速度的±15%区间
3、环境条件:A级区悬浮粒子控制在警戒限~行动限区间;模拟传递窗开启时间延长10秒
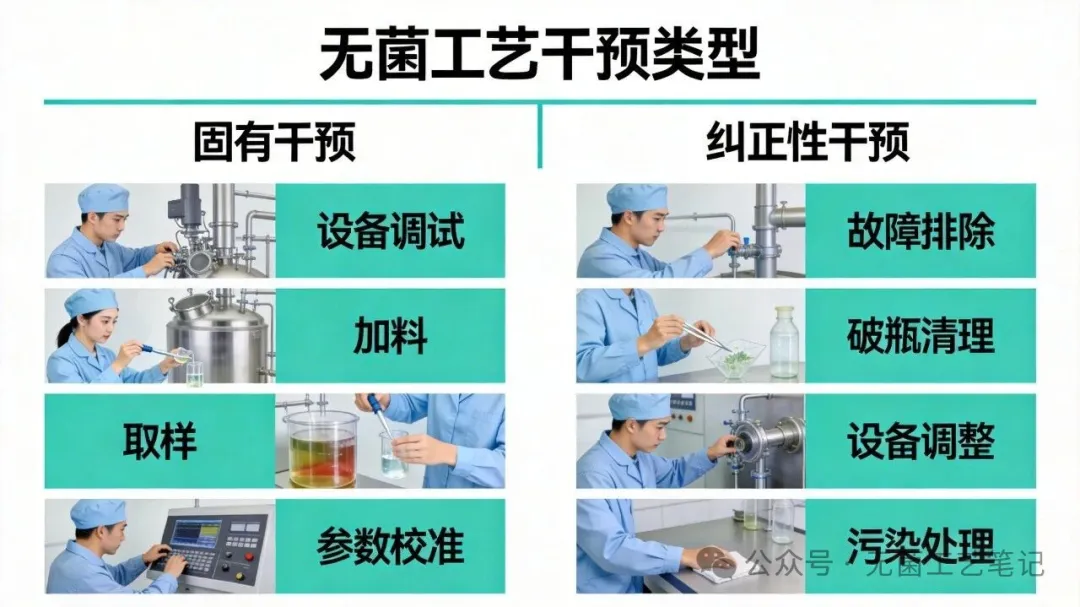
4、干预条件:固有干预每班次至少2次;纠正性干预每批次至少3次
4.3 批次规模要求
最大生产批量 | MFT批次规模 |
|---|---|
≥10000支 | ≥10000支 |
5000-10000支 | ≥最大生产批量 |
<5000支(如罕见药) | ≥3000支 |
个体化细胞治疗 | 总数≥最大批量的3倍 |
BFS生产线 | ≥3个连续循环,每循环≥1000个 |
五、常见问题与典型案例
5.1 常见问题
Q1:阴性对照污染怎么办?
A:立即终止试验!阴性对照污染说明培养基或器具灭菌存在问题,需全面调查后方可重新试验。
Q2:促生长试验失败怎么办?
A:该批次培养基不得使用。需调查原因(配制错误、灭菌过度、储存不当),重新配制并验证合格后方可用于试验。
Q3:新员工必须参加MFT吗?
A:是的。新员工入职不满3个月、刚通过无菌操作资质考核的,必须参与MFT以验证其操作能力。
5.2 典型案例分析
案例一:手套指尖污染导致MFT失败
某企业MFT试验中,一批次3000支出现1支阳性。经菌种鉴定为表皮葡萄球菌,来源于操作人员手套指尖。
根本原因:人员更衣程序确认不充分,手套消毒操作不规范。
纠正措施:重新培训无菌更衣操作,增加实操考核频次,增加手套指尖微生物监测频次。
案例二:设备密封性导致的污染
某冻干制剂生产线MFT中,出现2支阳性。调查发现灌装机针头密封圈老化,导致培养基泄漏。
根本原因:设备预防性维护计划未覆盖密封圈更换周期。
纠正措施:建立关键设备部件更换台账,将密封圈纳入关键备件管理,MFT前增加设备密封性检查项目。
六、行业趋势
6.1 法规趋严
近年来,无菌工艺验证的法规要求呈现全球化趋严趋势:
EU GMP Annex 1(2022版)首次引入污染控制策略(CCS)概念
FDA强化了对干预模拟和人员资质的要求
中国2025版GMP对培养基模拟灌装样本量、干预模拟提出更明确规定
6.2 技术革新
连续制造与PAT技术:过程分析技术(PAT)的应用,使无菌工艺过程控制更加精准
隔离器技术普及:隔离器(RABS、隔离舱)的广泛应用,显著降低了无菌工艺的污染风险
数字化与数据完整性:电子批记录(EBR)和计算机化系统的应用,对MFT数据管理提出更高要求
七、结语
培养基模拟灌装是制药企业无菌工艺能力的"照妖镜"——它不仅检验设备和环境,更检验人员、制度和管理。
一次合格的MFT,不仅是企业合规的证明,更是对患者用药安全的庄严承诺。
参考文献:
1,《药品生产质量管理规范(2023年修订)》附录1 无菌药品
2,《无菌工艺模拟试验指南(无菌制剂)》(征求意见稿)
3,PDA Technical Report No. 47 (Revised 2022)
4,EU GMP Annex 1: Manufacture of Sterile Medicinal Products (2022)
5,FDA Guidance for Industry: Sterile Drug Products Produced by Aseptic Processing
6,ISO 13408-1:2022
本文由环凯转载自“无菌工艺笔记”公众号,版权归原作者所有,仅供学习参考,如有侵权请联系删除!