GB/T 16294-2025 实施在即,医药洁净室沉降菌测试有哪些关键变化?
发布时间:2025-11-18 浏览次数:1033
医药工业洁净室(区)的微生物控制是药品质量安全的核心保障,而沉降菌测试作为直观反映空气微生物污染状况的关键手段,其标准化操作直接影响检测结果的准确性与可靠性。2025 年 10 月 5 日,国家市场监督管理总局与国家标准化管理委员会联合发布了新版《医药工业洁净室 (区) 沉降菌的测试方法》(GB/T 16294-2025),该标准将于 2026 年 11 月 1 日正式实施,全面替代 2010 年版标准。本文将深度解读新版标准的核心变化与实操要点,助力医药企业提前做好合规准备。
一、标准修订核心背景与适用范围
新版标准按照 GB/T 1.1-2020《标准化工作导则 第 1 部分:标准化文件的结构和起草规则》起草,聚焦医药工业洁净室(区)沉降菌测试的科学性与实操性。其适用范围覆盖医药工业洁净厂房、洁净实验室等各类洁净场所的沉降菌测试,是药品生产企业、医疗器械生产企业、检验检测机构开展微生物控制的重要技术依据。
本次修订结合行业发展需求与技术进步,对术语定义、测试条件、操作流程等关键内容进行优化,删除了部分过时要求,新增了更贴合实际应用的技术规范,进一步提升了标准的指导性与合规性。
二、新版标准核心技术变化解析
1. 术语定义更精准,统一行业认知
新版标准更新了 “沉降菌”“静态”“动态” 等核心术语定义。其中,“沉降菌” 明确为 “通过被动式采样法收集到的悬浮在空气中的活微生物”,“静态”“动态” 状态定义直接引用 GB/T 25915.1-2021 标准,确保了洁净室相关标准体系的一致性,避免了术语理解偏差导致的测试差异。
2. 新增培养基明确要求,强化检测基础
2010 年版标准未单独明确培养基要求,新版新增第 6 章 “培养基” 条款,规定常规测试优先选择胰酪大豆胨琼脂培养基(TSA),必要时可添加适宜中和剂。当监测结果疑似有真菌或受季节因素影响时,可增加沙氏葡萄糖琼脂培养基(SDA),且所有培养基需符合《中华人民共和国药典 2025 年版四部》9203 相关要求,从源头保障测试的有效性。
3. 采样点设定优化,突出风险评估导向
新版标准删除了 2010 年版 “最少培养皿数” 要求,改为 “基于风险评估确定采样点数目及位置”,并推荐使用 FMEA、HACCP 等风险管理工具。同时,明确了最少采样点数目底线(见表 1),面积超过 1000㎡的洁净室(区)需按公式计算(NL=3+(27×A/1000)/3,小数向上进位),且在浮游菌最少采样点数基础上增加 3 个,确保空间覆盖的全面性。
4. 采样与培养条件调整,贴合实际应用
采样时间:动态测试中,ISO5 级、A 级、B 级及 100 级洁净室(区)宜全程采样,其他级别基于风险评估确定;静态测试采样时间需与动态一致,单个培养皿暴露时间一般不超过 4h,避免培养基干燥或成分变质影响微生物存活。
培养条件:环境微生物种群不确定时,可采用 “20℃~25℃培养 3d~5d+30℃~35℃培养 2d~3d” 或反向组合模式;SDA 培养基培养温度为 20℃~25℃,时间延长至 5d~7d,可根据历史数据调整培养方案,提升菌落检出率。
5. 精简冗余条款,聚焦核心测试流程
新版标准删除了 2010 年版的 “结果计算”“结果评定”“日常监控”“采样点布置附录”“培养基灭菌及准备附录” 等内容。这一调整并非弱化要求,而是基于行业成熟经验,将结果评定等内容交由企业结合内控标准与产品特性制定,同时突出测试方法的核心操作流程,让标准更简洁易用。
三、企业合规实施关键准备事项
1. 人员培训与能力提升
组织测试人员学习新版标准,重点掌握风险评估工具应用、采样点优化设计、培养基选择与培养条件调整等新增要求,确保人员具备卫生与微生物学基础知识,且测试活动对洁净室(区)的干预降至最低。
2. 仪器与培养基合规配置
定期校准培养箱、压力蒸汽灭菌器等设备,确保符合标准要求;采购符合《中华人民共和国药典 2025 年版四部》9203 要求的 TSA、SDA培养基,必要时备好中和剂,建立培养基质量验证流程。
3. 测试流程优化与记录完善
结合企业洁净室(区)面积、洁净级别、生产工艺等,通过风险评估确定采样点数目与位置,制定个性化采样方案;完善试验报告内容,确保包含洁净室名称、占用状态、环境条件、采样点布置图、培养基种类、每个采样点沉降菌数等核心信息,实现测试全过程可追溯。
4. 过渡期衔接安排
在 2026 年 11 月 1 日实施前,企业可并行开展新旧标准对比测试,梳理差异点,调整现有测试流程与记录表单,避免标准切换导致的合规风险。
四、标准修订的行业意义
GB/T 16294-2025 的发布实施,是我国医药工业洁净室微生物控制标准化的重要进步。其核心意义在于:一是强化风险评估导向,让测试方案更贴合企业实际场景;二是统一技术要求,提升行业测试结果的可比性与公信力;三是精简冗余内容,降低企业合规成本;四是衔接药典与相关洁净室标准,完善医药行业标准化体系。
对于医药企业而言,及时落地新版标准要求,不仅是满足法规合规需求,更是提升产品质量安全保障能力、增强市场竞争力的关键举措。
五、核心变化对比表
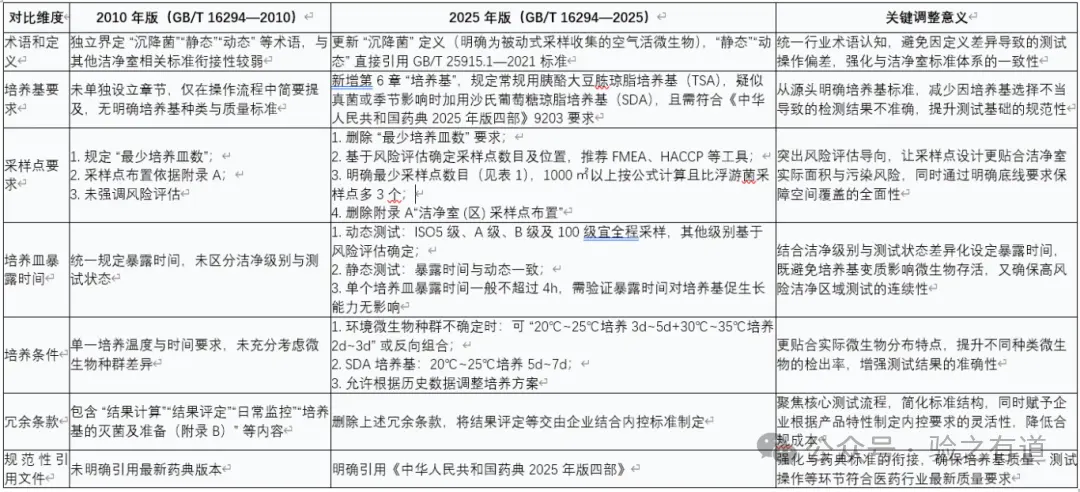
本文由环凯转载自“验之有道”公众号,版权归原作者所有,仅供学习参考,如有侵权请联系删除!