菌种传代“5代法则”全解析:从0代到5代计数模板与避坑指南
发布时间:2026-04-10 浏览次数:597
各位微生物室的老师,有没有过这种直击灵魂的瞬间:
- 飞检老师翻到你的菌种传代记录,指着标注的“3代工作菌”追问代次计算逻辑,你当场脑子一片空白?
- 室间质评药敏结果连续偏移,找遍了培养基、孵育条件的问题,最后发现是传了8代的金葡菌早就“变了性”?
- 刚复苏的冻干菌转种两次就慌了神:我这是不是快到5代红线了?甘油管复融一次,到底算不算传代?
在检验科微生物室,菌种就是我们手里的“标尺”。标尺不准,后续的鉴定、药敏、质控结果全都会跑偏。而《中国药典》里那句“工作菌株传代不得超过5代”,更是我们日常工作的红线,也是飞检、院感检查里的高频扣分点。
但现实是,90%的微生物人,都在传代这件事上踩过坑。今天我们就抛开生硬的法规条文,结合检验科日常操作,把“5代法则”的底层逻辑、计数误区、避坑方案一次讲透。
一、先搞懂:为什么检验科必须死卡“5代”这个数?
很多老师会疑惑:细菌十几分钟就分裂一次,5代分裂不过1小时,为什么药典要卡死“转种5次”的上限?
核心原因只有一个:控制菌种变异,守住我们检验结果的“金标准”。
我们日常用的ATCC25922、ATCC25923这些标准菌株,之所以能当质控的“尺子”,就是因为它的生化特性、耐药表型、生长特性都是固定的。但细菌每一次转种培养,都会伴随随机的自然突变,传代次数越多,突变累积得就越多,慢慢就会出现:
- 药敏质控的抑菌圈越跑越偏,甚至超出CLSI的允许范围;
- 生化鉴定反应变弱、甚至出现假阴性,导致鉴定结果错误;
- 阳性对照菌生长不良,让试验结果直接作废。
二、这些传代的基础认知,90%的人都搞混了
1,到底什么才算“0代菌”?别再把商业菌株当0代了!
药典明确规定:从认可的菌种保藏机构获得的冻干标准菌株,才是第0代。
这句话有两个核心要求,踩中一个就会出问题:
- 只有正规保藏机构的冻干菌株,才算0代。比如中检院、ATCC、CMCC这些具备合规保藏资质、完整溯源流程的机构,附带详细COA的冻干菌种,才是法定的0代起点。
- 商业公司售卖的“质控菌株”“定量菌株”“工作菌株”,哪怕吹得再天花乱坠,都不属于0代!它们属于商业派生菌株,它的COA上必须明确标注:原始0代菌株的溯源信息、自身的传代次数。
这里就是检验科最常见的天坑:很多老师买了商业菌株,默认它是0代,自己再转种4次,结果商业菌株本身已经是2代,加起来直接6代,超了红线还浑然不觉。
2,到底什么才算“一次传代”?这些边界一定要分清
药典对传代的定义是:将活的培养物接种到新鲜培养基中培养,任何形式的转种均被认为是传代1次。USP更是补充了核心前提:必须伴随微生物的生长增殖,才算一次有效传代。
1代:是指将活的培养物接种到新鲜培养基中,任何亚培养的形式均被认为是转重或传代一次。
冻干菌种(0代)→ 增菌培养18至24小时 苏醒(1代)→ 增菌培养18至24小时 复壮(2代)→ 划线传代(3代)
结合检验科日常操作,我们直接给大家划清边界,再也不用纠结:
✅ 算一次传代的情况:
- 冻干菌复融后划平板,孵育长出了单菌落(复融本身不算,长菌了才算);
- 甘油冻存管复融后,转种到平板/肉汤里,孵育后有细菌生长;
- 从平板上挑取菌落,接种到新鲜肉汤里增菌,肉汤里出现肉眼可见的浑浊生长。
❌ 不算传代的情况:
- 冻干菌仅复融,没有转种培养;
- 把菌液转到生理盐水、缓冲液里,没有提供生长条件,细菌没有增殖;
- 同一培养物,从肉汤划到平板上,没有再次转种到新的培养基,不算二次传代。
这里再纠正一个最常见的误区:细菌二分裂的“代”,和法规里的“传代”,完全是两码事。
细菌十几分钟分裂一次,是细胞增殖的代次;而法规里的传代,是“转种到新鲜培养基 → 完成一次生长周期”的完整过程,两者绝对不能混为一谈。
三、5代到底怎么算?给检验科一套可直接落地的计数模板
很多老师的传代记录混乱,核心是没有一套统一的计数逻辑。我们结合检验科最常用的“种子批-工作批”流程,给大家一套不会出错的计数示例,全科室可以直接写进SOP里:
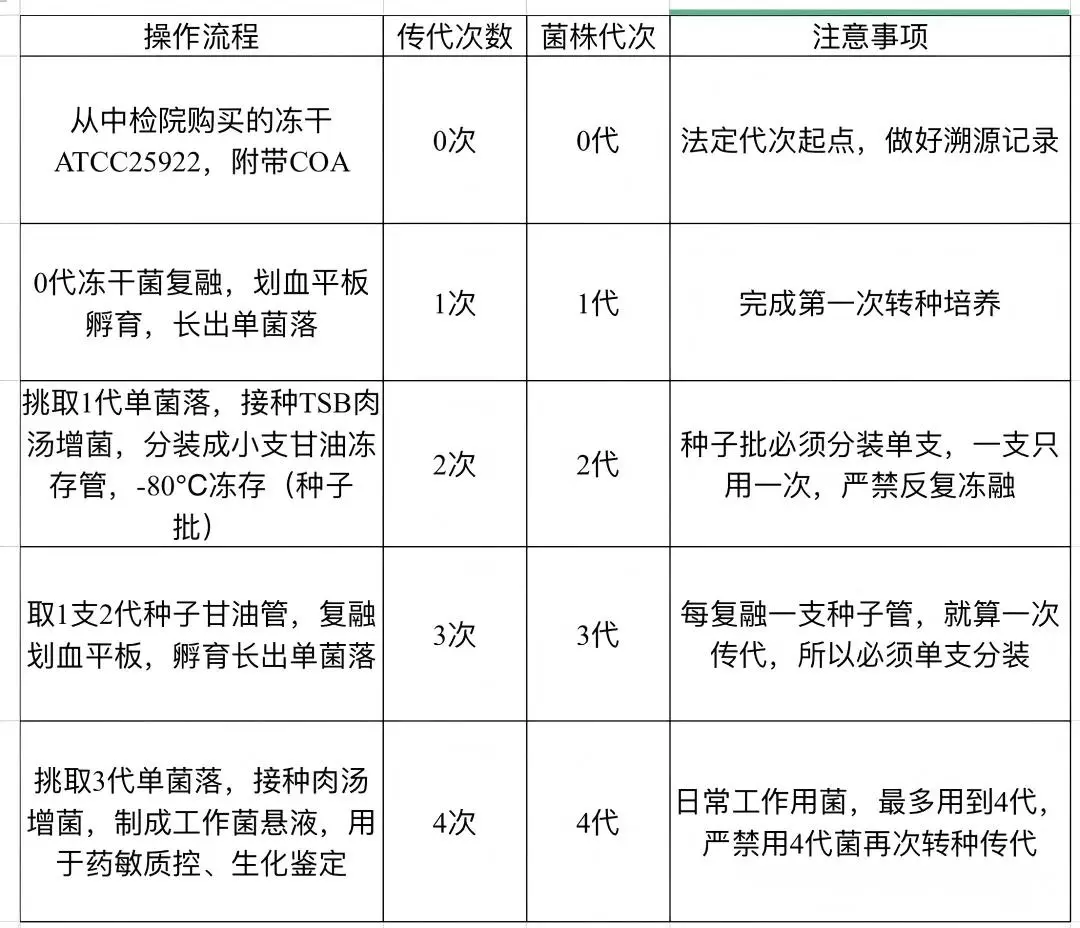
划重点:从0代开始,累计传代次数绝对不能超过5次。也就是说,我们日常用的工作菌,最多用到5代,再转种就超红线了。
强烈建议大家把工作菌的使用上限设为4代,留1次的缓冲空间,避免操作失误导致超线。
四、检验科传代最常踩的5个坑,看完直接避开
坑1:甘油管反复冻融,代次悄悄超线,最常见
这是最高发的错误!很多老师为了省事,把一整支甘油管反复冻融,每次用都拿出来划一次平板。但你每复融划一次平板,就算一次传代,一支甘油管用半年,代次早就超了5次,自己还不知道。
✅ 正确做法:种子菌必须分装成50-100μL的小支,一支只用一次,用完直接废弃,从根源避免反复冻融。
坑2:传代计数“一人一个标准”,全科室不统一
有的老师把“平板到肉汤”算1次,有的把“肉汤到平板”又算1次,同一支菌,不同人算出来的代次能差2代,检查的时候直接出问题。
✅ 正确做法:把传代计数规则写进SOP,全科室统一标准,每一次传代都做好双人核对,记录清晰可追溯。
坑3:只卡代次,不做菌种确认
很多老师觉得“只要传代在5代内就万事大吉”,但实际上,哪怕是3代菌,也可能出现变异。
✅ 正确做法:每传一代,都要做革兰染色、关键生化反应、药敏质控圈验证,确认菌株的特性和标准菌株一致,避免“尺子歪了”还在用。
坑4:商业菌株不看COA,代次从一开始就错了
买了商业质控菌株,不看COA上的原始传代次数,直接当0代用,结果本身已经是2代,自己再传3次就到了5代上限,再传就超线。
✅ 正确做法:所有商业菌株必须索要完整COA,明确原始溯源和传代次数,从它标注的代次开始往下计数,同时把菌株供应商纳入科室供应商管理。
坑5:传代操作不规范,人为加速菌株变异
很多老师传代的时候,随便挑一个菌落就传,或者传代的时候接种量过大,都会加速菌株的变异。
✅ 正确做法:每次传代必须挑取形态典型、大小均匀的单菌落,严格控制接种量,避免过度传代导致的选择压力,减少变异风险
五、最后想说
菌种传代的5代法则,从来不是束缚我们的条条框框,而是帮我们守住检验结果准确的底线。
我们微生物室出具的每一份鉴定报告、每一张药敏结果,背后都是患者的诊疗方案。而标准菌株,就是我们结果准确的第一道防线。只有把传代这件小事做严、做规范,我们手里的“尺子”才不会歪,出具的报告才够硬气。
各位老师在菌种传代的日常工作中,还遇到过哪些坑?欢迎在评论区留言交流,我们一起避坑,一起把微生物质控做扎实!

本文由环凯转载自“检言验语”公众号,版权归原作者所有,仅供学习参考,如有侵权请联系删除!